To tylko jedna z 13 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę

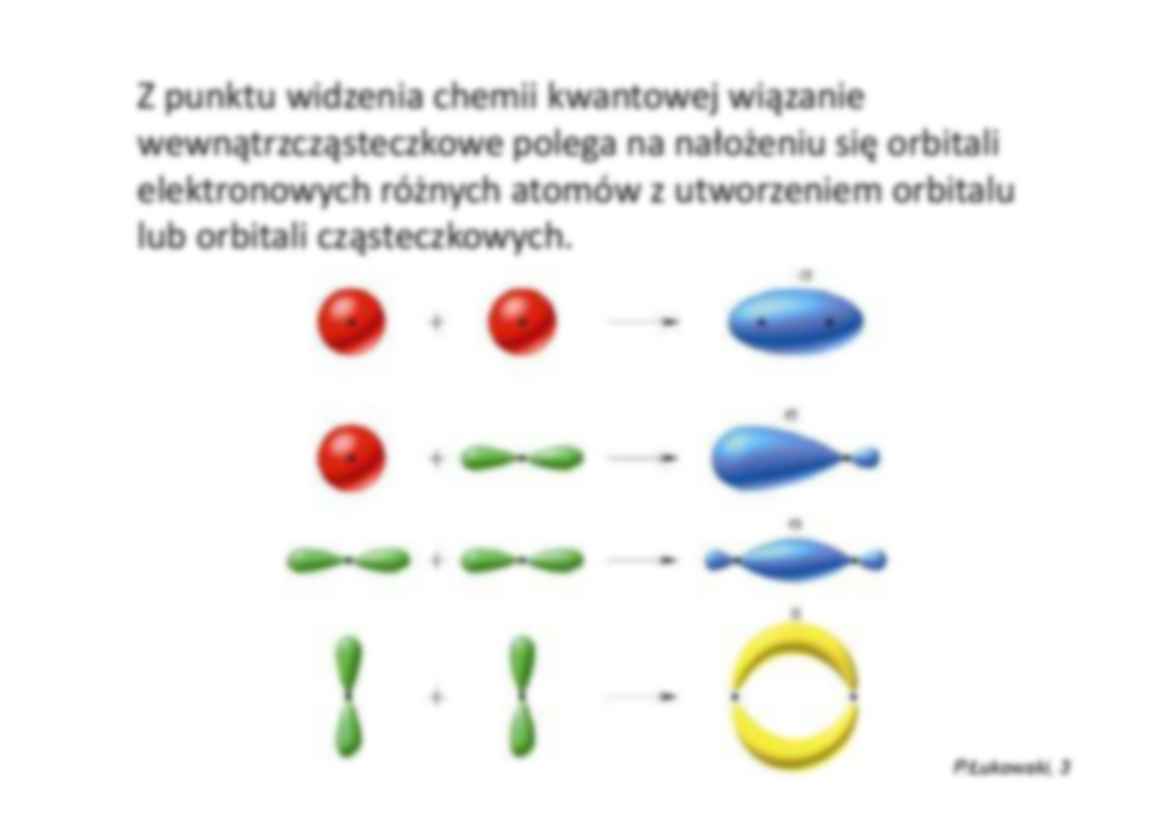
WIĄZANIA CHEMICZNE Wiązania I rzędu wewnątrzcząsteczkowe P.Łukowski, 2 Wiązanie chemiczne = siła wiążąca mniejsze elementy materii w większe struktury Wiązanie wewnątrzcząsteczkowe (I rzędu) = siła wiążąca atomy w cząsteczki P.Łukowski, 3 Z punktu widzenia chemii kwantowej wiązanie wewnątrzcząsteczkowe polega na nałożeniu się orbitali elektronowych różnych atomów z utworzeniem orbitalu lub orbitali cząsteczkowych. P.Łukowski, 4 Energia jonizacji, E j – miara łatwości, z jaką atom oddaje elektrony i staje się kationem: A + E j = K + + e– Powinowactwo elektronowe, E p – miara łatwości, z jaką atom przyłącza elektrony i staje się anionem: A + e– = A– + E p Elektroujemność, E u – miara zdolności atomu do przyciągania elektronów (im większa elektroujemność, tym silniej atom przyciąga elektrony): E u = Ej + Ep [keV] Elektroujemność w skali Paulinga (wielkość bezwymiarowa) = Eu / 6,3 P.Łukowski, 5 Elektroujemność pierwiastków w skali Paulinga Model tworzenia wiązania chemicznego P.Łukowski, 6 Zgodnie z zakazem Pauliego w jednym orbitalu – także orbitalu cząsteczkowym – mogą się znajdować dwa elektrony. Wiązanie może być utworzone przez parę elektronową . Reguła oktetu: każdy atom dąży do posiadania na powłoce walencyjnej 8 lub 0 elektronów (co umożliwia osiągnięcie stanu o najniższej energii). P.Łukowski, 7 Rodzaje wiązań wewnątrzcząsteczkowych Na Cl Na Cl Na Cl Na+ Cl– E u (Cl) = 3,2 Eu (Na) = 0,9 Elektron z powłoki walencyjnej sodu „przeskakuje” do powłoki walencyjnej chloru. Powstaje kation sodu i anion chloru, które przyciągają się elektrostatycznie. Jest to wiązanie jonowe. Jony Na+ i Cl– tworzą kryształ – „megacząsteczkę”. Nie istnieją pojedyncze cząsteczki NaCl – ten zapis oznacza tylko proporcję jednych jonów do drugich w związku chemicznym (1:1). P.Łukowski, 8 P.Łukowski, 9 Rodzaje wiązań wewnątrzcząsteczkowych Cl Cl Cl Cl Cl E u obu atomów są identyczne. Oba atomy przyciągają elektrony z jednakową siłą. Niesparowane elektrony zostają uwspólnione – tworzą wiążącą parę elektronową, znajdującą się dokładnie „pomiędzy” atomami chloru. Jest to wiązanie atomowe (kowalencyjne). Cl Cl Cl P.Łukowski, 10 Rodzaje wiązań wewnątrzcząsteczkowych B B B A B E u obu atomów różnią się nieznacznie. Jeden z atomów przyciąga elektrony nieco silniej.
(…)
…
P.Łukowski, 11
Rodzaje wiązań wewnątrzcząsteczkowych
W metalach występują rdzenie atomowe (atomy pozbawione
wszystkich elektronów z powłok walencyjnych) i gaz
elektronowy (zdelokalizowane elektrony walencyjne).
Jest to wiązanie metaliczne.
P.Łukowski, 12
Rodzaje wiązań wewnątrzcząsteczkowych
H
H N
H+
Gdy oba elektrony w wiążącej
parze elektronowej pochodzą od
tego samego atomu.
H
H
H N H+
H
Jest to wiązanie koordynacyjne
(donorowo-akceptorowe)
np. jon amonowy NH4+
P.Łukowski, 13
…
... zobacz całą notatkę






Komentarze użytkowników (0)