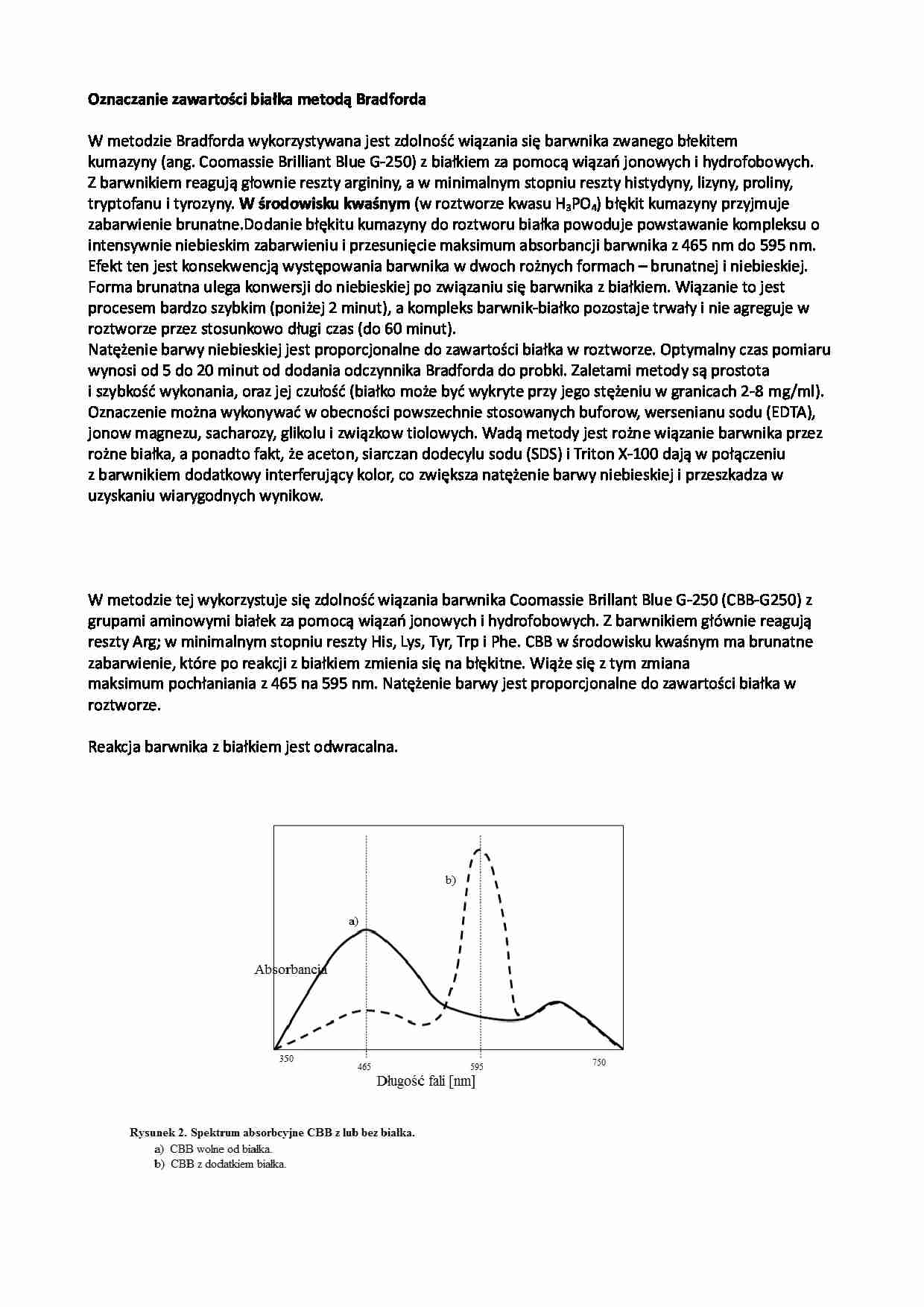
Oznaczanie zawartości białka metodą Bradforda W metodzie Bradforda wykorzystywana jest zdolność wiązania się barwnika zwanego błekitem kumazyny (ang. Coomassie Bril iant Blue G-250) z białkiem za pomocą wiązań jonowych i hydrofobowych. Z barwnikiem reagują głownie reszty argininy, a w minimalnym stopniu reszty histydyny, lizyny, proliny, tryptofanu i tyrozyny. W środowisku kwaśnym (w roztworze kwasu H3PO4) błękit kumazyny przyjmuje zabarwienie brunatne.Dodanie błękitu kumazyny do roztworu białka powoduje powstawanie kompleksu o intensywnie niebieskim zabarwieniu i przesunięcie maksimum absorbancji barwnika z 465 nm do 595 nm. Efekt ten jest konsekwencją występowania barwnika w dwoch rożnych formach – brunatnej i niebieskiej. Forma brunatna ulega konwersji do niebieskiej po związaniu się barwnika z białkiem. Wiązanie to jest procesem bardzo szybkim (poniżej 2 minut), a kompleks barwnik-białko pozostaje trwały i nie agreguje w roztworze przez stosunkowo długi czas (do 60 minut). Natężenie barwy niebieskiej jest proporcjonalne do zawartości białka w roztworze. Optymalny czas pomiaru wynosi od 5 do 20 minut od dodania odczynnika Bradforda do probki. Zaletami metody są prostota i szybkość wykonania, oraz jej czułość (białko może być wykryte przy jego stężeniu w granicach 2-8 mg/ml). Oznaczenie można wykonywać w obecności powszechnie stosowanych buforow, wersenianu sodu (EDTA), jonow magnezu, sacharozy, glikolu i związkow tiolowych. Wadą metody jest rożne wiązanie barwnika przez rożne białka, a ponadto fakt, że aceton, siarczan dodecylu sodu (SDS) i Triton X-100 dają w połączeniu z barwnikiem dodatkowy interferujący kolor, co zwiększa natężenie barwy niebieskiej i przeszkadza w uzyskaniu wiarygodnych wynikow. W metodzie tej wykorzystuje się zdolność wiązania barwnika Coomassie Bril ant Blue G-250 (CBB-G250) z grupami aminowymi białek za pomocą wiązań jonowych i hydrofobowych. Z barwnikiem głównie reagują reszty Arg; w minimalnym stopniu reszty His, Lys, Tyr, Trp i Phe. CBB w środowisku kwaśnym ma brunatne zabarwienie, które po reakcji z białkiem zmienia się na błękitne. Wiąże się z tym zmiana maksimum pochłaniania z 465 na 595 nm. Natężenie barwy jest proporcjonalne do zawartości białka w roztworze. Reakcja barwnika z białkiem jest odwracalna.
... zobacz całą notatkę



Komentarze użytkowników (0)