

Fragment notatki:
1.Zasady Termodynamiki-definicje, wzory, wykresy. *0 zasada termodynamiki = istnienie temperatury empirycznej;
ciało w równowadze termodynamicznej ma wszędzie tą samą temperaturę, oraz jeżeli 3 układy A, B i C mogą się wymieniać ciepłem, to są one w równowadze termodynamicznej.
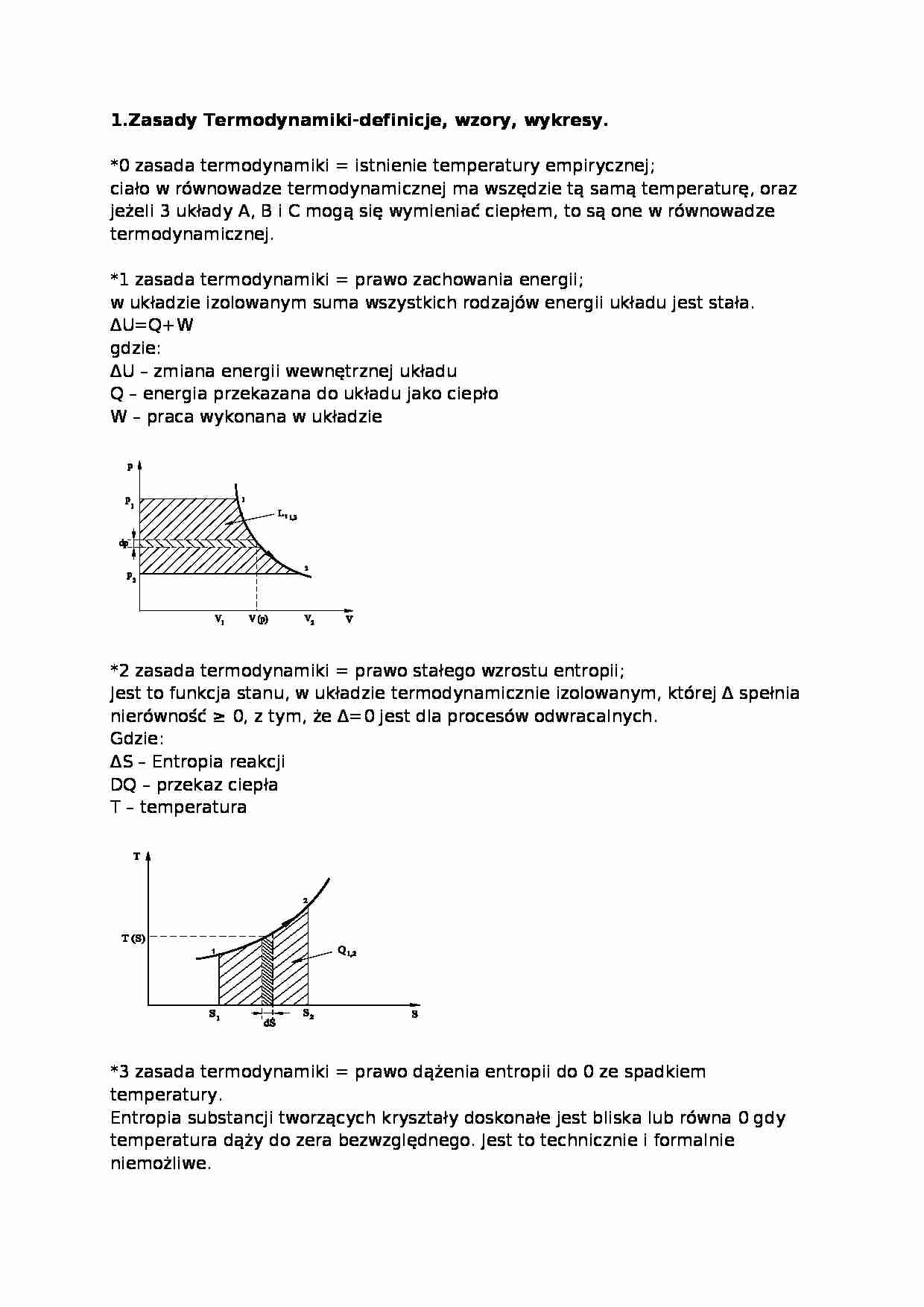
*1 zasada termodynamiki = prawo zachowania energii;
w układzie izolowanym suma wszystkich rodzajów energii układu jest stała.
ΔU=Q+W
gdzie:
ΔU - zmiana energii wewnętrznej układu
Q - energia przekazana do układu jako ciepło
W - praca wykonana w układzie
*2 zasada termodynamiki = prawo stałego wzrostu entropii;
Jest to funkcja stanu, w układzie termodynamicznie izolowanym, której Δ spełnia nierówność ≥ 0, z tym, że Δ=0 jest dla procesów odwracalnych.
Gdzie:
ΔS - Entropia reakcji
DQ - przekaz ciepła
T - temperatura
*3 zasada termodynamiki = prawo dążenia entropii do 0 ze spadkiem temperatury.
Entropia substancji tworzących kryształy doskonałe jest bliska lub równa 0 gdy temperatura dąży do zera bezwzględnego. Jest to technicznie i formalnie niemożliwe.
2. Destylacja- co to jest, rodzaje i zastosowanie . Destylacja jest to proces rozdzielania ciekłej mieszaniny związków chemicznych przez odparowanie, a następnie skroplenie jej składników. Stosuje się ją w celu wyizolowania lub oczyszczenia jednego lub więcej związków składowych.
Główny produkt destylacji - czyli skroplona ciecz nazywana jest destylatem. Pozostałość po destylacji nazywana jest cieczą wyczerpaną.
Destylacja prosta - polega na jednorazowym odparowaniu i skropleniu cieczy
Destylacja wielostopniowa - seria destylacji prostych, prowadzonych jedna po drugiej
Rektyfikacja - destylacja kaskadowa, w aparaturze, która umożliwia automatyczne, wielokrotne odparowywanie i skraplanie cieczy; stosowana głównie w laboratoriach, a w szczególności w przemyśle chemicznym, fermentacyjnym i farmaceutycznym
Destylacja próżniowa - destylacja prowadzona pod obniżonym ciśnieniem. Ten sposób prowadzenia procesu destylacji zaliczany jest do tzw. zachowawczych metod rozdziału substancji. Dzięki obniżeniu ciśnienia możliwe jest obniżenie temperatury wrzenia destylowanej cieczy, co ma szczególnie duże znaczenie w przypadku, gdy któraś z rozdzielanych substancji jest podatna na rozkład termiczny.
Obniżanie ciśnienia wiąże się też jednak ze zmniejszaniem się różnic w temperaturach wrzenia rozdzielanej mieszaniny, stąd destylację próżniową można prowadzić dla związków chemicznych o znacznych różnicach tych temperatur. Podział destylacji próżniowej dokonywany jest na podstawie wartości zastosowanego ciśnienia.
(…)
….
W przemianach jonowych podczas rozrywania wiązania atomowego para elektronowa zostaje przy jednym z powstających fragmentów, który staje się karboanionem, drugi zaś karbokationem. Zachodzi wówczas, gdy atomy różnią się między sobą elektroujemnością. Heterolityczny rozpad wiązań niekoniecznie musi powodować utworzenie się karbokationów lub karboanionów istniejących jako niezależne elementy. Najczęściej nowe…
… i produktów nie korelują się ze sobą, to takie reakcje są zabronione ze względu na symetrię orbitali molekularnych.
6. Przedstawić mechanizm organicznych reakcji rodnikowych.
W reakcjach rodnikowych pary elektronowe tworzące wiązania kowalencyjne (atomowe) ulegają rozerwaniu w taki sposób, że przy każdym z powstających fragmentów zostaje jeden niesparowany elektron. Zachodzi to w przypadku, gdy atomy…
… hipsochromowe - charakteryzują się brakiem wiązań podwójnych i wolnych par elektronowych.
…
…, polisacharyd, o cząsteczkach złożonych z kilkunastu do kilkuset tysięcy jednostek glukozy połączonych β-1,4-wiązaniami glikozydowymi. Celuloza jest podstawowym składnikiem ścian komórkowych roślin. W stanie czystym jest białym proszkiem o gęstości ok. 1,5 g/cm3).
9. Porównać aldehydy i ketony.
Aldehydy - związki organiczne posiadające grupę aldehydową lub formaldehydową, której atom jest bezpośrednio związany…
… do alkoholi I-rzędowych, utlenianie do kwasów karboksylowych
Ketony - grupa związków organicznych zawierających grupę karbonylową (C=0) połączoną z dwona atomami węgla.
Właściwości (zbliżone do aldehydów): ketony z niewielkimi grupami alkilowymi są cieczami (dobrze mieszają się z wodą), związki bardzo polarne, niiereaktywne, często stosowane jako rozpuszczalniki
Otrzymywanie: katalityczne odworodnienie II…
… również do określania właściwości redukujących cukrów. Monosacharydy oraz większość disacharydów dają pozytywny wynik próby. Przykładem disacharydu niewykazującym właściwości redukujących jest sacharoza (produkty jej hydrolizy dają wynik pozytywny). Polisacharydy w większości wykazują wynik negatywny.
Obydwie próby sotsowane są do wykrywania glukozy w roztworach.
6. Przedstawić mechanizm jonowych reakcji organicznych…
… do tego szkieletu atomów wodoru. Atomy węgla łączą się ze sobą tworząc łańcuchy proste lub rozgałęzione oraz pierścienie. Węglowodory dzielimy (ze względu na ilość wiązań) na:
- nasycone(bez wiazań podwojnych i potrojnych): alkany - nienasycone (z podwojnymi i potrojnymi): alkeny, alkiny i węglowodory aromatyczne
lub ze względu na topologię łańcuchów:
- liniowe - w których występują ściśle liniowe łańcuchy węglowe…
… bezpośrednio z atomami węgla w pierścieniu aromatycznym
Właściwości: odczyn lekko kwaśny, ulegają dysocjacji elektrolitycznej, reagują z metalami aktywnymi (wydziela się wodór), reagują z wodorotlenkami i tlankami zasadowymi, odbarwiaja wodę bromową, ulegaja nitryfikacji i sulfonowaniu
Identyfikacja: za pomocą soli żelaza (III) barwy pomarańczowej
Otrzymywanie: hydroliza chlorowcopochodnych arenów, metoda…
... zobacz całą notatkę

Komentarze użytkowników (0)