To tylko jedna z 5 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


WYKŁAD 8_1 Równowagi fazowe ciecz-ciało stałe
1. Równowagi fazowe w układach skondensowanych ( ciecze i ciała stałe ).
Ciśnienie stałe i duŜe, aby nie było fazy gazowej.
Układem czysta substancja stała i jej nasycony roztwór ciekły [np. naftalen(1) i jego nasycony roztwór
w benzenie(2)].
∗
c
Warunek równowagi fazowej tylko dla naftalenu, bo tylko naftalen jest w obu fazach: µ1s = µ1
c
∗
∗
∗
Zakładając, Ŝe roztwór ciekły jest doskonały µ1 = µ1 c + RT ln x 1 otrzymuję: µ1s = µ1 c + RT ln x 1
∗
∗
Gs
Gc
µ1 s − µ1 c
= R ln x 1 czyli m1 − m1 = R ln x 1
T
T
T
G
∂ ∂G ∗ T − 1 ∗ G
− S∗ T − G − S∗T − H + S∗ T − H
T
=
=
= 2
Uwzględniając, Ŝe dla kaŜdego G = ∂T
2
∂T
T
T2
T2
T
Równanie równowagi fazowej róŜniczkuję względem temperatury przy stałym ciśnieniu:
d ln x 1
− Hs 1 Hc 1
Gs 1 Gc 1
∂
c
s
m
m
+ m =R∗
; a poniewaŜ H 1m − H 1m = ∆H top1
− m = R ln x 1
⇒
2
2
T
T
dT
∂T p
T
T
Dzieląc obie strony przez T otrzymuję:
to:
d ln x 1 ∆H top1
=
i całkując to równanie względem temperatury w granicach Ttop do bieŜącej T otrzymuję
dT
RT 2
∆H top1 1
1
ln x 1 =
∗
− równanie Hildebrandta – van Laara gdzie ∆H top1 0 zawsze.
Ttop1 T
R
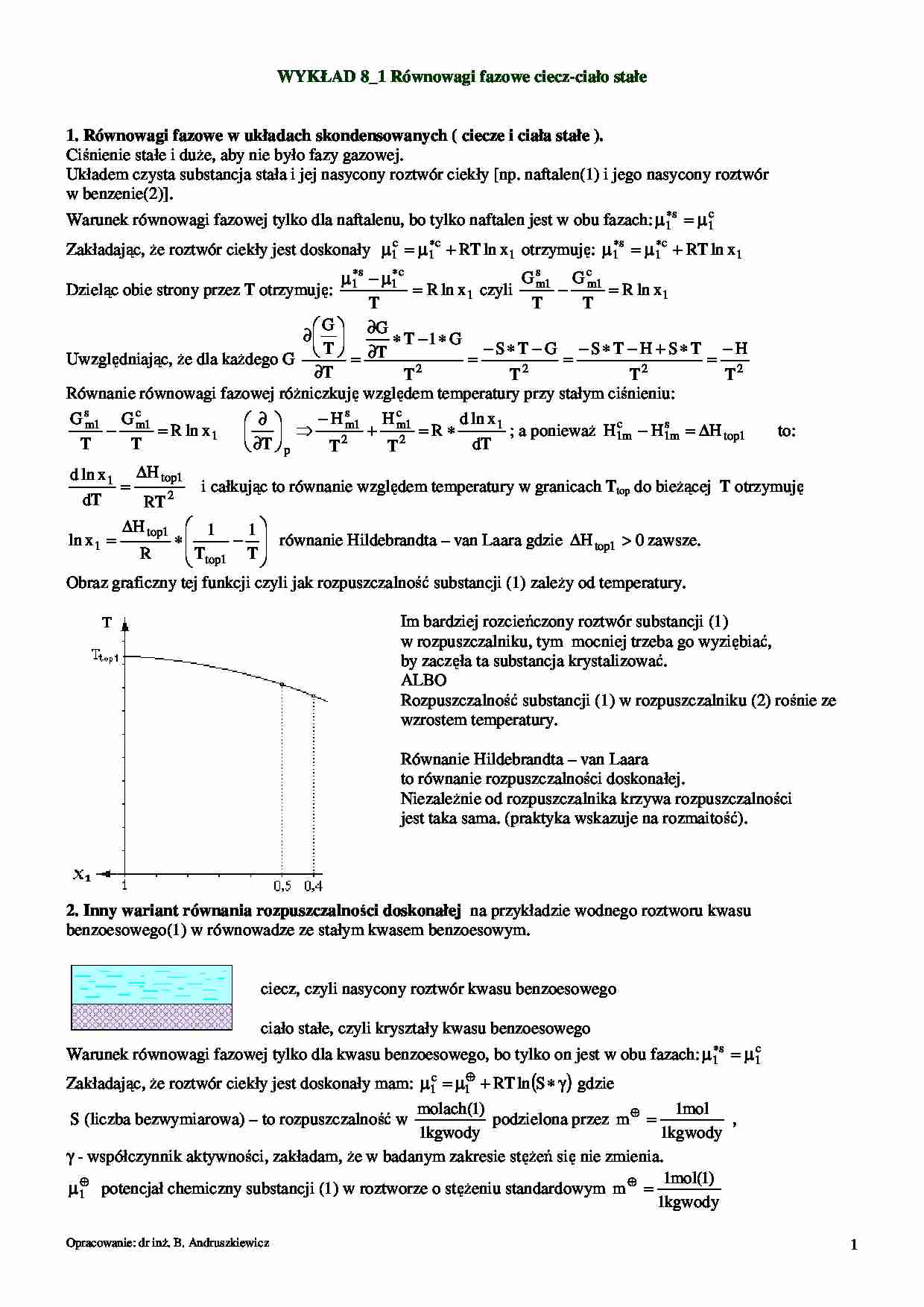
Obraz graficzny tej funkcji czyli jak rozpuszczalność substancji (1) zaleŜy od temperatury.
Im bardziej rozcieńczony roztwór substancji (1)
w rozpuszczalniku, tym mocniej trzeba go wyziębiać,
by zaczęła ta substancja krystalizować.
ALBO
Rozpuszczalność substancji (1) w rozpuszczalniku (2) rośnie ze
wzrostem temperatury.
Równanie Hildebrandta – van Laara
to równanie rozpuszczalności doskonałej.
NiezaleŜnie od rozpuszczalnika krzywa rozpuszczalności
jest taka sama. (praktyka wskazuje na rozmaitość).
2. Inny wariant równania rozpuszczalności doskonałej na przykładzie wodnego roztworu kwasu
benzoesowego(1) w równowadze ze stałym kwasem benzoesowym.
ciecz, czyli nasycony roztwór kwasu benzoesowego
ciało stałe, czyli kryształy kwasu benzoesowego
∗
c
Warunek równowagi fazowej tylko dla kwasu benzoesowego, bo tylko on jest w obu fazach: µ1s = µ1
c
⊕
Zakładając, Ŝe roztwór ciekły jest doskonały mam: µ1 = µ1 + RT ln (S ∗ γ ) gdzie
molach(1)
1mol
S (liczba bezwymiarowa) – to rozpuszczalność w
podzielona przez m ⊕ =
,
1kgwody
1kgwody
γ - współczynnik aktywności, zakładam, Ŝe w badanym zakresie stęŜeń się nie zmienia.
1mol(1)
⊕
µ1 potencjał chemiczny substancji (1) w roztworze o stęŜeniu standardowym m ⊕ =
1kgwody
Opracowanie: dr inŜ. B. Andruszkiewicz
1
∗
⊕
Wracając do warunku równowagi fazowej mam: µ1s = µ1 + RT ln S
∗
⊕
µ1 s − µ1
G roztwór G s 1
Dzieląc obie strony przez T otrzymuję:
= R ln(S ∗ γ ) czyli m1
− m = − R ln(S ∗ γ )
T
T
T
G
∂
−H
T
Uwzględniam, Ŝe dla kaŜdego G = 2
∂T
T
Równanie równowagi fazowej róŜniczkuję względem temperatury przy stałym ciśnieniu:
G roztwór G s 1
m1
− m = − R ln(S ∗ γ )
T
T
H roztwór H s
d ln S
∂
⇒ m12 − m1 = R ∗
;
2
∂T p
dT
T
T
roztwór
s
a poniewaŜ H1m
− H1m = ∆H rozp1
to:
∆H rozp1 1
d ln S ∆H rozp1
=
i całkując to równanie względem temperatury
(…)
… nad ciepłem solwatacji.
−
∆H rozp1
=
3. Eutektyk to układ dwuskładnikowy dwufazowy ciecz – ciało stałe , w którym:
- roztwór ciekły jest doskonały ( µ i = µ ∗ + RT ln x i )
i
- a w stanie stałym składniki tworzą odrębne fazy.
Ogólnie mówiąc, faza gazowa zawsze jedna bez względu na to, czy składnik jeden czy składniki dwa w układzie,
fazy ciekłe mogą być dwie – gdy duŜe odchylenia dodatnie. W fazie stałej…
… temperatura topnienia
składnika 2
TN temperatura topnienia
naftalenu
TB temperatura topnienia benzenu
TE temperatura eutektyczna
∆Htop1 entalpia topnienia
składnika 1
∆Htop2 entalpia topnienia
składnika 2
∆HtopN entalpia topnienia
naftalenu
∆HtopB entalpia topnienia benzenu
∆HN entalpia topnienia naftalenu
∆HB entalpia topnienia benzenu
xB ułamek molowy benzenu
xN ułamek molowy naftalenu
xEB ułamek molowy benzenu w
mieszaninie eutektycznej
xEN ułamek molowy benzenu w
mieszaninie eutektycznej
Opracowanie: dr inŜ. B. Andruszkiewicz
T temperatura, w której ciecz o
składzie xB jest w równowadze ze
stałym benzenem (punkt na
krzywej, stęŜenie roztworu
nasyconego względem benzenu w
wybranej temperaturze)
T temperatura, w której ciecz o
składzie xń jest w równowadze ze
stałym naftalenem.
3
Zadanie 2 zjazdu 8_1…
... zobacz całą notatkę






Komentarze użytkowników (0)