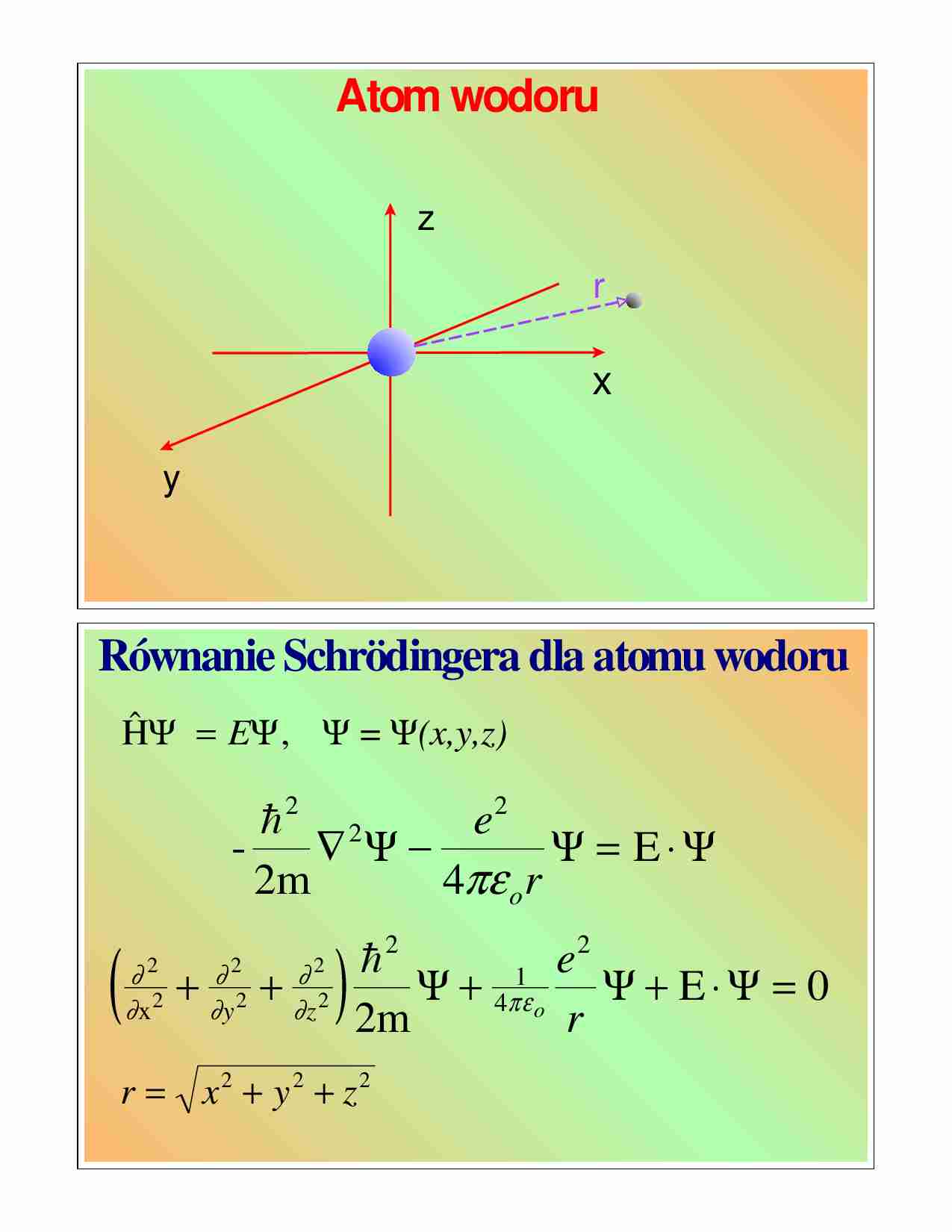
Atom wodoru
z
r
x
y
Równanie Schrödingera dla atomu wodoru
$
HΨ = EΨ , Ψ = Ψ(x,y,z)
h2 2
e2
∇ Ψ−
Ψ = E⋅Ψ
2m
4πε o r
(
∂
∂ x2
2
+ ∂∂y 2 + ∂∂z2
2
2
)
h2
e2
1
Ψ + 4πε o Ψ + E ⋅ Ψ = 0
2m
r
r = x2 + y2 + z2
Równanie Schrödingera dla atomu wodoru (c.d.)
∂ Ψ
∂ x2
2
+
∂ Ψ
∂ y2
2
+
∂ Ψ
∂ z2
2
2m
+ 2 ⋅ E +
h
1
Ψ = 0
2
2
2
x + y +z
e2
4π ε o
!!!
NIE DA SIĘ ROZWIĄZAĆ ANALITYCZNIE !!
Układ współrzędnych
z
h
M
r
n
y
x
W układzie
współrzędnych
kartezjańskich:
xM, yM, zM
W układzie współrzędnych
biegunowych sferycznych:
r, h, n
Układ współrzędnych (2)
r = x2 + y2 + z2
z
ϑ = arccos
r
xM = r@cosn@sinh
yM = r@sinn@sinh
zM = r@cosh
z
h
M
r
n
x
ϕ = arccos 2
2
x +y
x
y
Równanie Schrödingera dla atomu wodoru (3)
Po zamianie układu współrzędnych na biegunowe sferyczne:
∂Ψ
∂ 2 ∂Ψ ∂
1
1 ∂ 2Ψ
2
sin ϑ ∂r r ∂r + ∂ϑ sin ϑ ∂ϑ + sin ϑ ∂ϕ 2 +
r ⋅ sin ϑ
2m
e2
+ 2 E +
Ψ = 0
h
4πε o ⋅ r
NIE UCZYĆ SIĘ NA PAMIĘĆ !!!
Obejrzeć i zapomnieć ...
Rozwiązanie r. Schrödingera dla atomu
wodoru
*R(r)*2dr
prawdopodobieństwo radialne,
elektron pomiędzy r a r + dr
*Y(h,n)*2 MhMn prawdopodobieństwo kątowe,
elektron w kierunku pomiędzy
h a h+Mh oraz n a n+Mn
Równanie Schrödingera dla atomu wodoru (2)
Q(x,y,z) = Q(r,h,n)
hn
Q(r,h,n) = R(r)@Y(h,n)
hn
@ hn
Rozdzielenie zmiennych w równaniu
róŜniczkowym = rozdział na kilka równań
WARUNEK KONIECZNY:
Q(r,h,n) JEST
hn
FUNKCJĄ PORZĄDNĄ
R(r)
Y(h,n) SĄ
hn
TAKśE KLASY Q
Warunki dla funkcji klasy Q (1)
muszą być spełnione, Ŝeby rozwiązanie dla atomu wodoru
składało się z funkcji porządnych
Energia całkowita moŜe przybierać tylko
pewne wartości:
πme e
const
E=−
= 2
2 2
2ε o h n
n
4
gdzie n = 1,2,3, .......
GŁÓWNA LICZBA KWANTOWA
Warunki dla funkcji klasy Q (2)
r
r r
Moment pędu: M = m × v × r
Moment pędu elektronu moŜe przybierać tylko
pewne wartości:
M = l(l + 1 )h
gdzie l = 0,1,2, ..... (n-1)
POBOCZNA LICZBA KWANTOWA
ORBITALNA LICZBA KWANTOWA
Warunki dla funkcji klasy Q (3)
Moment pędu moŜe mieć tylko pewne orientacje
w przestrzeni, tj. jego składowa w wybranym
kierunku osi z moŜe przybierać pewne wartości:
Mz = m⋅ h
gdzie m = -l, -l + 1,....,0, .....l - 1, l
MAGNETYCZNA LICZBA KWANTOWA
Wartości energii całkowitej
n=7
n=4
n=3
Energia
elektronu
n=2
n=1
Moment pędu i jego składowa Mz
l =2
l =3
z
z
3£
2£
£
0
-£
-2£
-3£
2£
£
0
-£
-2£
m = 0,±1,±2
m = 0,±1,±2,±3
Liczby kwantowe
n
1
2
3
4
l
0
0
1
0
1
2
0
1
2
3
m
0
0
-1,0,+1
0
-1,0,+1
-2,-1,0,+1,+2
0
-1,0,+1
-2,-1,0,+1,+2
- 3,-2,-1,0,+1,+2+3
KaŜda kombinacja liczb odpowiada jednej funkcji falowej
... zobacz całą notatkę





Komentarze użytkowników (0)