To tylko jedna z 21 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę

efekt izotopowy - procesy różnicowania/rozdziału składu izotopowego
pierwiastka pomiędzy co najmniej dwiema substancjami (dwoma
fazami zwierającymi ten sam pierwiastek)
reakcje wymiany izotopowej (efekt termodynamiczny) - proces
równowagowy w układzie zamkniętym; pomimo iż substancje
wymieniają pomiędzy sobą izotopy, różnica stosunków izotopowych
pomiędzy tymi substancjami nie ulegnie zmianie,
procesy kinetyczne - zależne głównie od różnic tempa reakcji izotopów
lżejszych i cięższych, zachodzące w układzie otwartym.
Proces (destylacja) Rayleigha – układ jednostronnie otwarty
Batch – układ zamknięty
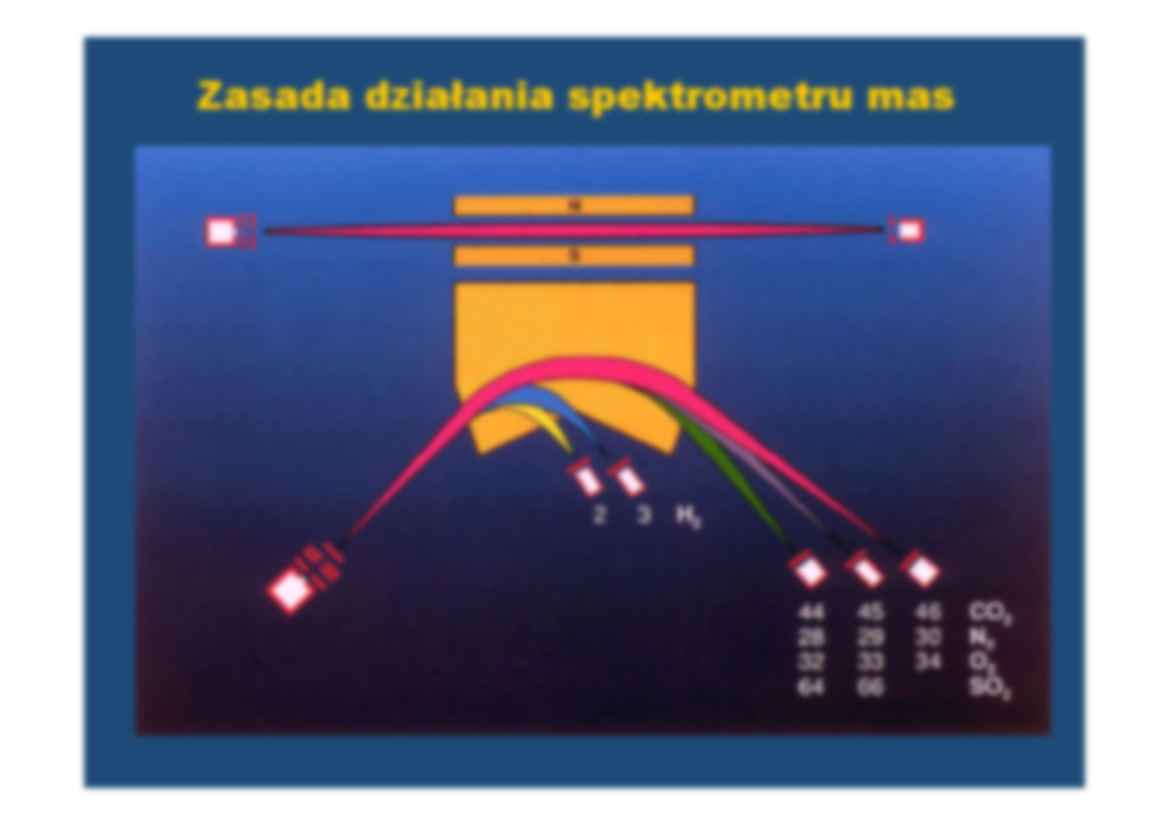
Zasada działania spektrometru mas
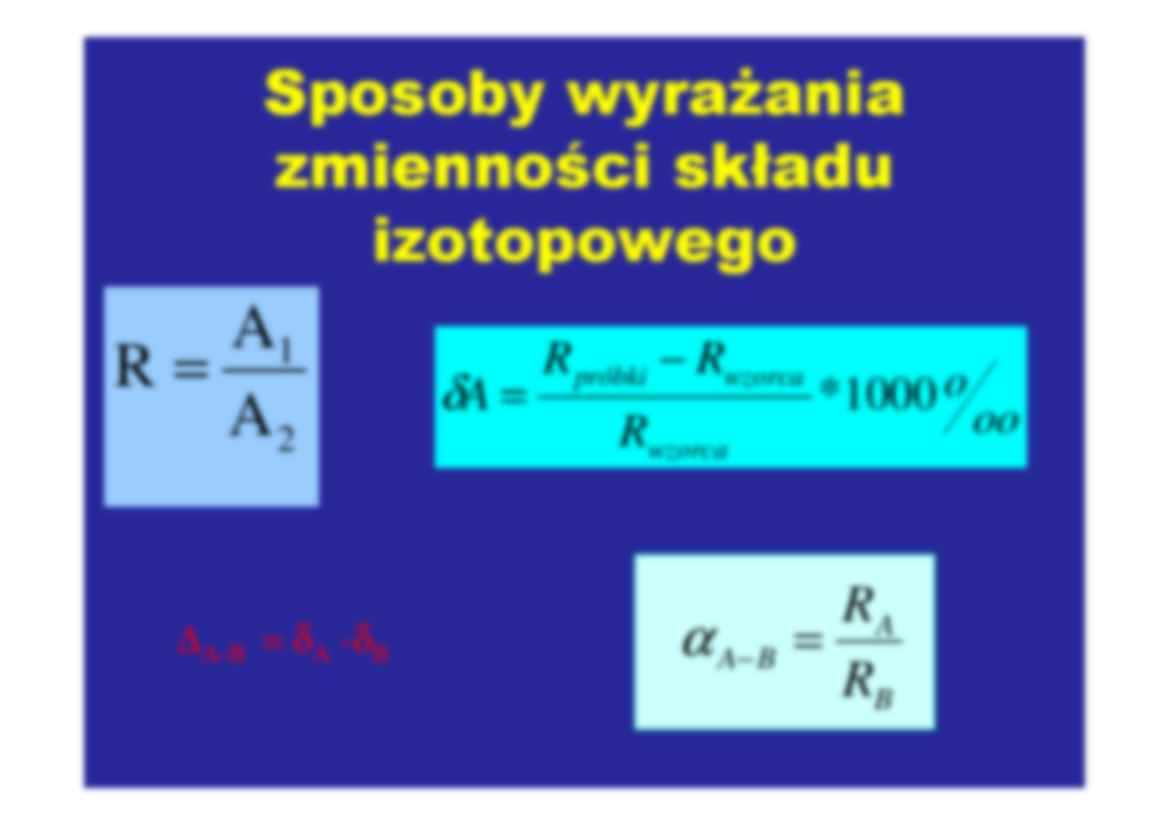
Sposoby wyrażania
zmienności składu
izotopowego
A1
R próbki − Rwzorca
R=
δA =
*1000 o
oo
A2
Rwzorca
∆A-B = δA -δB
α A− B
RA
=
RB
CO POWINIEN ZROBIĆ STUDENT I ROKU OCHRONY ŚRODOWISKA W
SEMESTRZE LETNIM 2006 BY ZDAĆ ZALICZENIE Z TEGOZ
WYKŁADU
1.
2.
3.
4.
5.
6.
Uważnie notować słowo po słowie wszystko co Pan profesor powiedział.
Analizować zapisane informacje, nie wspominając już o tym, żeby
uczęszczać na każdy wykład, a nie bezmyślnie kserować notatki od
dobrodusznych kolegów z roku.
W razie wątpliwości czy niezrozumienia tematu - pytać, pytać i jeszcze raz
pytać o wszystko o czym mowa na wykładach.
Konsultować się z kolegami lepszymi od siebie, by dopełnić swoją wiedzę i
ją ugruntować.
Każdy wykres zauważony na slajdach natychmiast zapisywać na twardym
dysku swojego mózgu i zabezpieczyć hasłem przed włamaniem przez osoby,
bądź informacje zbędne i niepowołane. Dla bezpieczeństwa skopiować na
papier.
Bez względu na okoliczności pójść na pierwszy termin zaliczenia, bo potem
może być już tylko gorzej!
Rad dla potomnych udzieliła
Agnieszka, studentka I roku Ochrony Środowiska.
Kilka rad jak uniknąć strat
1.Wykład
-czas poświęcony Ci na nim dany Ci jest tylko raz ,więc należycie go
spożytkuj.
-problemy omawiane na wykładzie wiążą się ze sobą ,abyś i Ty mógł je
powiązać bądź na wykładach od początku.
-uważnie patrz i słuchaj, siedzenie z przodu na pewno to ułatwi.
-zwracaj szczególną uwagę na wykresy i wartości na nich przyjęte.
-zadawaj pytania
2.Nauka
-warto po każdym wykładzie, lub w niedługim czasie po nim aczkolwiek
koniecznie przed następnym-wypracuj samodyscypline.
-po pół rocznej chcianej bądź też nie integracji nie jesteś sam(chyba...)
więc pytaj koleżanki i kolegów o ich tok myślenia bo Twój niekoniecznie może
być poprawny.
-prowadź przejrzyste notatki, porównując je z notatkami innych.
3.Egzamin
-nie zakładaj, że zdasz aczkolwiek po zastosowaniu się do powyższych rad i
własnych metod, które sa dla ciebie najlepsze nie powinno byæ z tym
problemu.
Sławek
pozostala para [frakcja]
0.75
0.25
0.00
11 ‰
-10
8
δ18O
[‰]
0.50
kondensat
9‰
1.00
0
para
-20
-30
1.00
0.75
0.50
0.25
pozostala para [frakcja]
0.00
Woda morska
Średnio ok. 0 ‰
Zatoki, intensywne parowanie, dopływ wód słodkich
δD
+/15 ‰, czasem –40 ‰
δ18O +/1,3 ‰ , czasem ???
Kondensat, w temperaturze 20oC, wzbogacony jest w
(…)
… do lekkiego,
Rp - początkowy stosunek izotopu ciężkiego do lekkiego,
f - pozostała ilość związku w układzie,
α - współczynnik frakcjonowania izotopowego
Model destylacji Rayleigha opisuje m.in.:
-stopień zaawansowania reakcji w układzie
otwartym czyli ilość materii, jaka została
odprowadzona z układu,
dotyczy rozdziału faz, efektów
izotopowych, oraz np. ????
Zakres składu izotopowego siarki
w różnych średowiskach przyrodniczych
meteoryty
S wulkaniczna
skały osadowe
woda oceaniczna
ewaporaty
ropa naftowa
powietrze
jon siarcznowy - wody powierzchniowe
węgiel kamienny
gleba
-60
-40
-20
0
δ S [‰]
34
20
40
60
1000
tem
mperatura [C]
800
600
400
200
0
0
5
10
1000 ln a
15
20
1000
900
temp
peratura [oC]
800
Frakcjonowanie
izotopowe tlenu
700
600
A - plagioklaz-woda
B - amfibol-woda
C - ilmenit-woda
D - magnetyt…
…
+/15 ‰, czasem –40 ‰
δ18O +/1,3 ‰ , czasem ???
Kondensat, w temperaturze 20oC, wzbogacony jest w izotop
cięższy względem pary o 9 ‰, a w temperaturze około
0oC o 11 ‰.
W miarę postępu skraplania pary wodnej pozostała para jest
zubażana w izotop cięższy (18O), czyli powstający
kondensat ma coraz niższą wartość δ18O (czy zarówno
każda nowa porcja jak i kondensat jako całość?).
W miarę zmniejszania…
... zobacz całą notatkę






Komentarze użytkowników (0)