e n c y k lo p e d ia P W N : zw ią zk i ko or dy na cy jn e, zw ią zk i ko m pl ek so we , ko m pl ek sy , zw ią zk i ch em icz ne o zło żo ny ch cz ąs te cz ka ch lu b jo na ch ,w kt ór yc h at om lu b jo n (k at io n) ,z wa ny at om em lu b jo ne m ce nt ra ln ym ,j es tz wi ąz an y wi ąz an ie m ko or dy na cy jn ym z tz w. lig an da m i; np .w cz ąs te cz ce K 3 [F e( CN ) 6] ,k at io n że la za je st jo ne m ce nt ra ln ym ,a an io ny cy ja nk ow e są lig an da m i. at om ce nt ra ln y, jo n ce nt ra ln y, at om bą dź jo n st an ow ią cy rd ze ń ko m pl ek su (z wi ąz ku ko or dy na cy jn eg o) i pr zy łą cz aj ąc y pe wn ą lic zb ę jo nó w uj em ny ch lu b cz ąs te cz ek ob oj ęt ny ch ,z wa ny ch lig an da m i; np .w ko m pl ek sie ka rb on ylk u że la za , Fe (C O ) 5, at om ce nt ra ln y je st at om że la za . W ik ip e d ia : A c o m p le x i n c h em is tr y u su al ly i s u se d t o d es cr ib e m o le cu le s o r en se m b le s fo rm ed b y t h e co m b in at io n o f li g an d s an d m et al i o n s. O ri g in al ly , a co m p le x i m p li ed a r ev er si b le a ss o ci at io n o f m o le cu le s, at o m s, o r io n s th ro u g h w ea k ch em ic al b o n d s. A s ap p li ed to co o rd in at io n ch em is tr y , th is m ea n in g h as e v o lv ed . S o m e m et al c o m p le x es a re f o rm ed v ir tu al ly i rr ev er si b ly an d m an y ar e b o u n d to g et h er b y b o n d s th at ar e q u it e st ro n g . T h e io n s o r m o le cu le s su rr o u n d in g t h e m et al a re c al le d l ig an d s. L ig an d s ar e g en
(…)
… encyklopedia PWN:
związki koordynacyjne, związki kompleksowe, kompleksy, związki
chemiczne o złożonych cząsteczkach lub jonach, w których atom lub jon
(kation), zwany atomem lub jonem centralnym, jest związany wiązaniem
koordynacyjnym z tzw. ligandami; np. w cząsteczce K3[Fe(CN)6], kation
żelaza jest jonem centralnym, a aniony cyjankowe są ligandami.
atom centralny, jon centralny, atom bądź jon stanowiący rdzeń
kompleksu (związku koordynacyjnego) i przyłączający pewną liczbę
jonów ujemnych lub cząsteczek obojętnych, zwanych ligandami; np. w
kompleksie karbonylku żelaza, Fe(CO)5, atom centralny jest atom
żelaza.
A complex in chemistry usually is used to describe molecules or ensembles formed by the
combination of ligands and metal ions. Originally, a complex implied a reversible association
of molecules, atoms, or ions through weak chemical bonds. As applied to coordination
chemistry, this meaning has evolved. Some metal complexes are formed virtually irreversibly
and many are bound together by bonds that are quite strong. The ions or molecules
surrounding the metal are called ligands. Ligands are generally bound to a metal ion by a
coordinate covalent bond (donating electrons from a lone electron pair into an empty metal
orbital), and are thus said to be coordinated to the ion. The areas of coordination chemistry
can be classified according to the nature of the ligands, broadly speaking (tylko część
przykładów):
− Classical (or "Werner Complexes"): Ligands in classical coordination chemistry bind to
metals, almost exclusively, via their "lone pairs" of electrons residing on the main group
atoms of the ligand. Typical ligands are H2O, NH3, Cl-, CNExample: [Co(EDTA)]-] {ethylenediaminetetraacetic acid, kwas
etylenodiaminotetraoctowy,}, [Co(NH3)6]Cl3
Wikipedia:
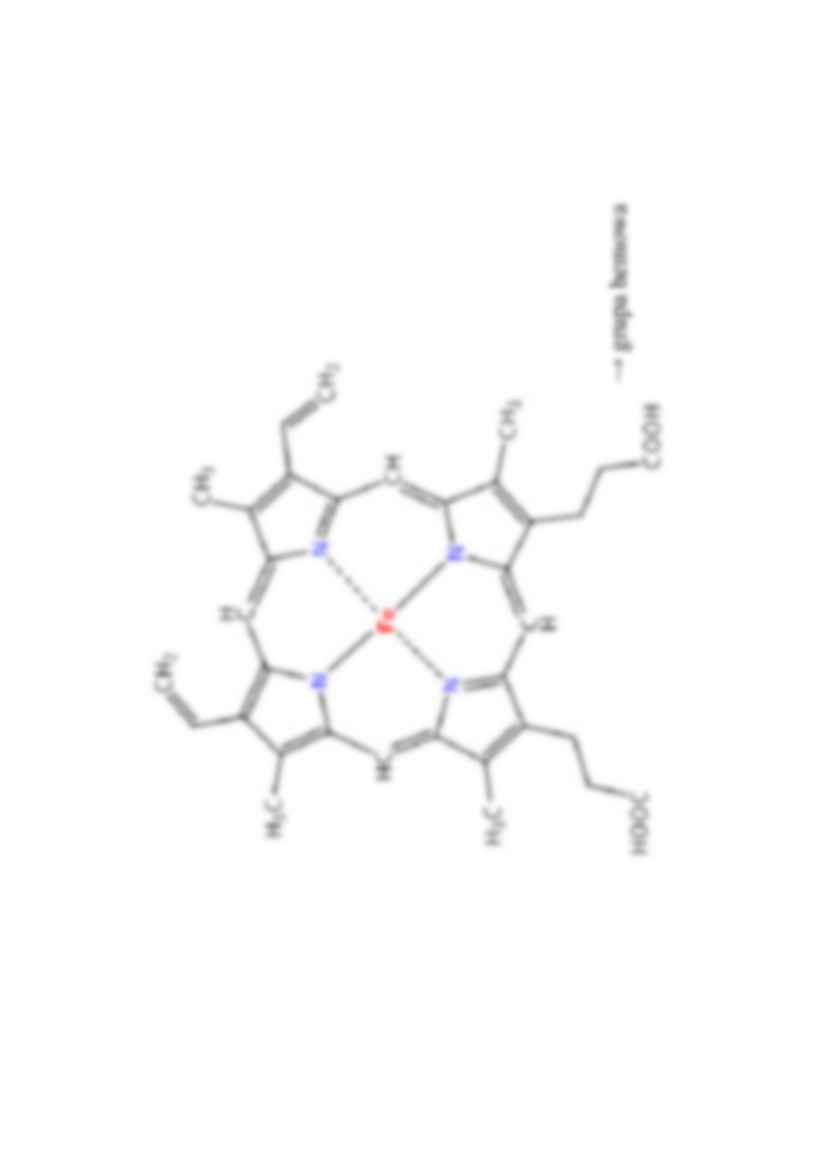
→ grupa hemowa
…
... zobacz całą notatkę





Komentarze użytkowników (0)