To tylko jedna z 10 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


W Ę G L O W O D O R Y A R O M A T Y C Z N E - ARENY
BENZEN
Benzen został odkryty przez Faradaya w 1825 r. w oleistej pozostałości w londyńskich, ulicznych
lampach oświetlanych gazem.
Michał Faraday (1791-1867); ur. W Newington Butts, Surrey, Wielka Brytania, dyrektor
laboratoriu w Royal Institution, prof. chemii w Royal Institution.
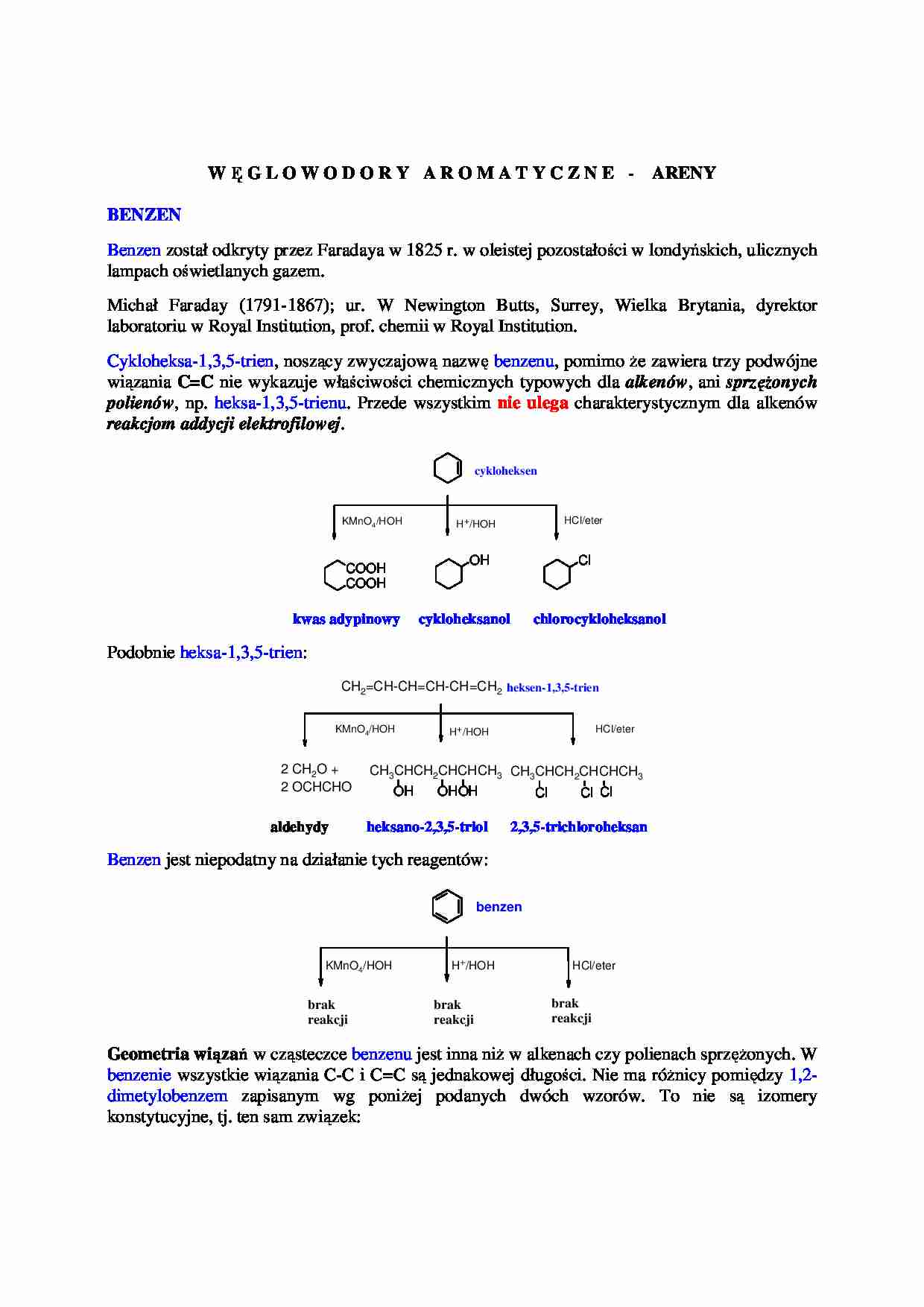
Cykloheksa-1,3,5-trien, noszący zwyczajową nazwę benzenu, pomimo Ŝe zawiera trzy podwójne
wiązania C=C nie wykazuje właściwości chemicznych typowych dla alkenów, ani sprzęŜonych
polienów, np. heksa-1,3,5-trienu. Przede wszystkim nie ulega charakterystycznym dla alkenów
reakcjom addycji elektrofilowej.
cykloheksen
KMnO4/HOH
HCl/eter
H+/HOH
OH
COOH
COOH
kwas adypinowy
Cl
cykloheksanol
chlorocykloheksanol
Podobnie heksa-1,3,5-trien:
CH2=CH-CH=CH-CH=CH2 heksen-1,3,5-trien
KMnO4/HOH
2 CH2O +
2 OCHCHO
aldehydy
HCl/eter
H+/HOH
CH3CHCH2CHCHCH3 CH3CHCH2CHCHCH3
OH
OHOH
heksano-2,3,5-triol
Cl
Cl Cl
2,3,5-trichloroheksan
Benzen jest niepodatny na działanie tych reagentów:
benzen
KMnO4/HOH
brak
reakcji
H+/HOH
brak
reakcji
HCl/eter
brak
reakcji
Geometria wiązań w cząsteczce benzenu jest inna niŜ w alkenach czy polienach sprzęŜonych. W
benzenie wszystkie wiązania C-C i C=C są jednakowej długości. Nie ma róŜnicy pomiędzy 1,2dimetylobenzem zapisanym wg poniŜej podanych dwóch wzorów. To nie są izomery
konstytucyjne, tj. ten sam związek:
H
CH3
H
H
H
H
H
H
H
H
H
H
H
H
CH3 H
H
H
benzen
CH3
H
H
H
H
CH3
1,2-dimetylobenzen
kąty w pierścieniu = 120o.
długość wiązania C-C = C=C = 1,39 Å;
Występowanie
Węglowodory aromatyczne i inne związki organiczne zawierające układ aromatyczny są
rozpowszechnione w przyrodzie, wiele z nich pełni waŜne funkcje biochemiczne:
CH2CHCOOH
H3C OH
OH
NH2
NH2
fenyloalanina
aminokwas
OH
CH2CHCOOH
H
HO
H3CNH
OH
tyrozyna
aminokwas
H
H
CH3
HO
efedryna,
alkaloid
H
CH2NHCH3 HO
adrenalina
neuroprzenośnik
H
HO
O
N CH3
H
HO
estradiol
Ŝeński hormon
płciowy
morfina,
narkotyk
alkaloid (lek)
Źródła węglowodorów aromatycznych
Węglowodory aromatyczne występują w ropie naftowej, w zaleŜności od jej gatunków w
mniejszej lub większej ilości. Znajdują się w smole pogazowej – produkcie
wysokotemperaturowej pirolizy węgla kopalnego. Wydajność smoły pogazowej wynosi 3-4%
wsadu węglowego. Obok smoły pogazowej w produktach pirolizy węgla znajduje się gaz (np. gaz
koksowniczy) i koks. Gas koksowniczy po ochłodzeniu ulega częściowo skropleniu i ta ciekła
frakcja nazywa się benzolem surowym. Znajduje się w niej głównie benzen (70%) i toluen
(~15%). Smołę pogazową – bogate źródło arenów – poddaje się destylacji na frakcje i zaleŜności
od lotności wydziela się: benzen, toluen, ksyleny, etylobenzen, polialkilowane benzeny, kumen,
naftalen, inden, antracen i wyŜsze areny oraz pochodne węglowodorów aromatycznych, np.
fenole, aminy aromatyczne, pirydyna i inne.
CH3
CH3
CH3
CH3
CH3
CH3
toluen
CH2CH3
o-ksylen
m-ksylen
CH3
p-ksylen
etylobenzen
Areny powstają z
... zobacz całą notatkę






Komentarze użytkowników (0)