WYKŁAD 1_1
1. Układ - otoczenie
Układ to część świata, która jest przedmiotem naszych zainteresowań (w danej chwili ). Reszta świata to otoczenie.
Układ ma ściśle zdefiniowane granice – niekoniecznie rzeczywiste powierzchnie, czasem tylko powierzchnie pomyślane.
UKŁAD
IZOLOWANY
∆m=0; ∆U=0
UKŁAD
ZAMKNIĘTY
∆m=0; ∆U≠0
UKŁAD
OTWARTY
∆m≠0; ∆U≠0
Stan układu to jego sytuacja opisana zespołem informacji umoŜliwiających odtworzenie go dowolną ilość razy.
Ten zespół informacji to parametry stanu ( n1, n2, T, p )
2. Równowaga termodynamiczna czyli wszystkie właściwości układu stałe w czasie dowolnie długim:
-równowaga mechaniczna - nie ma sił niezrównowaŜonych -tłok się nie porusza, ciśnienia wyrównane;
-równowaga termiczna
- nie ma róŜnic temperatur;
-równowaga chemiczna - stęŜenia wszystkich składników stałe w czasie i we wszystkich miejscach.
3. Zerowa zasada termodynamiki.
Dwa róŜne układy kontaktują się przez ściankę: sztywną( nie dopuszczającą do wyrównywania ciśnień),
nieprzepuszczalną (nie ma wymiany masy), diatermiczną (pozwalającą na wymianę ciepła). Jeśli zetknąć takie
wybrane dwa układy, to początkowo zachodzić będzie proces wymiany ciepła, potem wszystkie właściwości się ustalą i
juŜ nic dziać się nie będzie. Układy będą w równowadze termicznej.
Jeśli układ A jest w równowadze termicznej z układem P(próbnik), oraz jeśli układ D jest w równowadze
termicznej z układem P(próbnik), to ( bez sprawdzania moŜna być pewnym ) układ A jest w równowadze
termicznej z układem D.
Stąd wniosek - jest jedna wielkość charakteryzująca stan równowagi termicznej. Nazwano ją TEMPERATURA.
RóŜnica temperatur to miernik oddalenia od stanu równowagi termicznej.
4. Termodynamiczna skala temperatur
Zaobserwowano, Ŝe dla wszystkich gazów granica iloczynu pV zaleŜy od temperatury - jest do niej wprost
proporcjonalna.
lim (pV) = R ∗ T
p →0
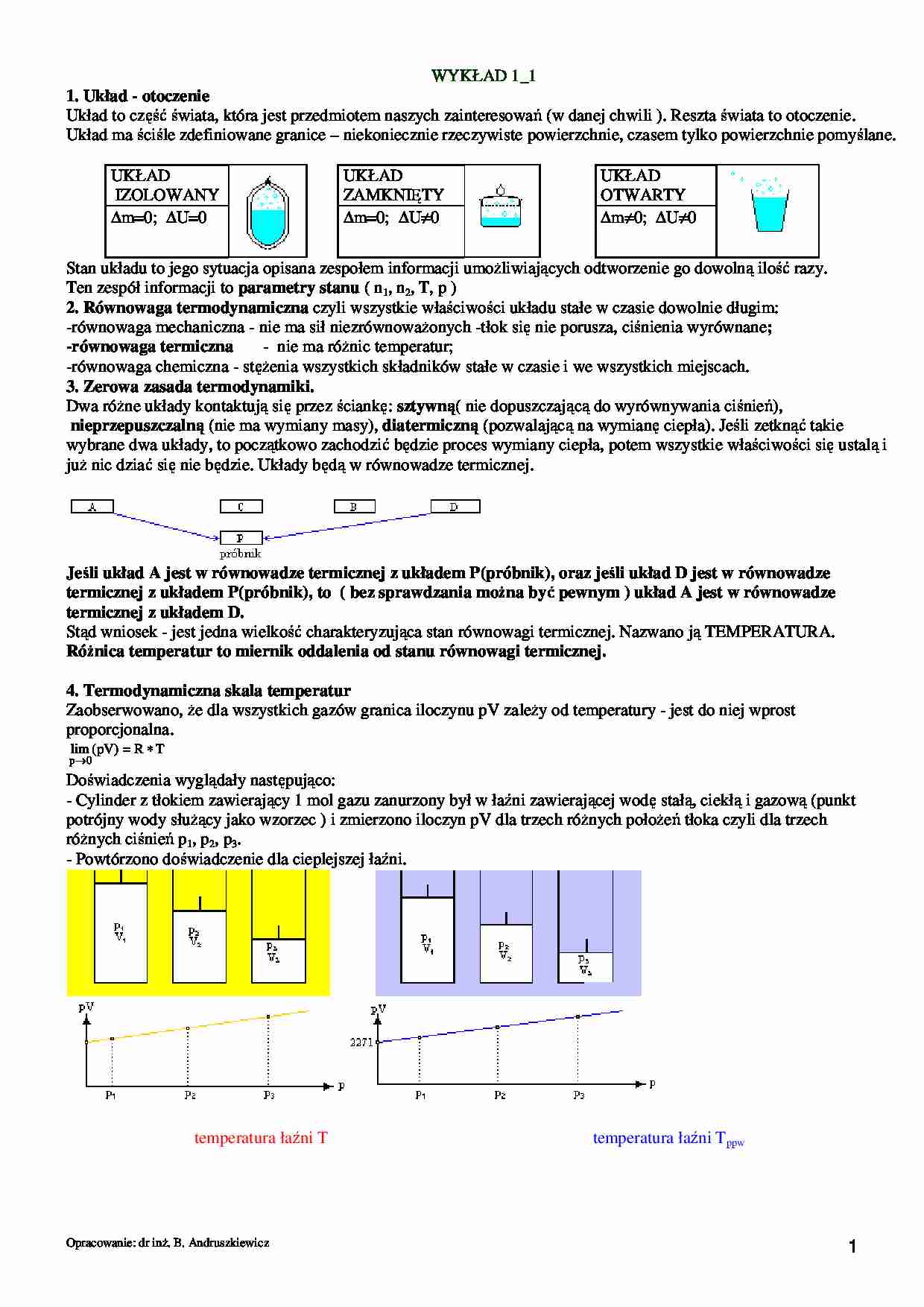
Doświadczenia wyglądały następująco:
- Cylinder z tłokiem zawierający 1 mol gazu zanurzony był w łaźni zawierającej wodę stałą, ciekłą i gazową (punkt
potrójny wody słuŜący jako wzorzec ) i zmierzono iloczyn pV dla trzech róŜnych połoŜeń tłoka czyli dla trzech
róŜnych ciśnień p1, p2, p3.
- Powtórzono doświadczenie dla cieplejszej łaźni.
temperatura łaźni T
Opracowanie: dr inŜ. B. Andruszkiewicz
temperatura łaźni Tppw
1
Sporządzono wykresy pV=f(p) i odczytano przez ekstrapolację lim (pV) ppw = 2271
p →0
większa od
N∗m
2271
mol
N∗m
mol
oraz lim (pV) T (jakaś liczba, tutaj
p →0
bo łaźnia Ŝółta cieplejsza od niebieskiej).
Sytuacja współistnienia wszystkich trzech stanów skupienia wody
(punkt potrójny wody) niech będzie wzorcowa dla tej wielkości – temperatury.
lim (pV) ppw = R ∗ Tppw
p →0
czyli
2271
N∗m
J
= 8,314
∗ 273,16K
mol
mol ∗ K
gdzie 2271 to wartość eksperymentalna.
Przypisano tej temperaturze(Tppw) wartość 273,16K, wtedy stała proporcjonalności R ma wartość 8,314J/molK.
Przypisanie Tppw = 273,16K powoduje, Ŝe K (kelvin, jednostka na skali temperatury termodynamicznej) to taka sama
róŜnica temperatur jak stopień
(…)
… wszystkich rodzajów energii w układzie.
- energia jądrowa, elektronowa, energia wiązań chemicznych,
- energia ruchu translacyjnego cząsteczek,
- energia ruchu rotacyjnego cząsteczek,
- energia ruchu oscylacyjnego cząsteczek,
- energia oddziaływań międzycząsteczkowych, itd., itp.
Absolutna wartość energii wewnętrznej nieznana (nie do zmierzenia), ale do zmierzenia są zmiany energii
wewnętrznej.
∆U→w całej przemianie od 1 do 2; dU→w róŜniczkowym fragmencie przemiany
→
U(V,T) energia wewnętrzna jako funkcja dwu zmiennych.
∆U = U2 –U1 stan końcowy minus stan początkowy.
Bez względu jaką drogą dokonuje się przejście od (1) do (2) ∆U jest ciągle takie samo
ENERGIA WEWNĘTRZNA JEST FUNKCJĄ STANU.
8. Pierwsza zasada termodynamiki
∆U=Q+w dU=Qel +wel
Q – energia wymieniona między układem a otoczeniem na sposób ciepła…
… IZOCHORYCZNA
2.Para wodna o temp. 100°C i
o p=1atm skrapla się i na końcu jest
ciecz o temp.100°C i p=1atm
2.Gaz (T1 ,p ,V1 ) w ilości 1mola
zamknięty w zbiorniku z ruchomym
tłokiem ogrzewano aŜ jego objętość
wzrosła do V2 (T2 ,p ,V2).
PRZEMIANA IZOBARYCZNA
.
itd
1. W stałej temperaturze i pod
stałym ciśnieniem
w miejsce substratów pojawiają
się produkty
CaCO 3 → CaO + CO 2
3.Gaz (p1 ,V1 , T) w stałej temp…
... zobacz całą notatkę





Komentarze użytkowników (0)