To tylko jedna z 42 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


Enzymologia
E
l i
Wykład 13
Wykład 13
Reakcje hydrolityczne
j y
y
Nitryle w przyrodzie
Nitryle w przyrodzie
Związki
Z i ki organiczne zawierające grupę nitrylową powstają nie t lk j k
i
i j
it l
t j
i tylko jako
produkty naturalne, ale też w wyniku aktywności człowieka.
Naturalne nitryle są produkowane przez rośliny bakterie grzyby algi owady
rośliny, bakterie, grzyby, algi, owady,
jedynym wyjątkiem są ssaki. Są często metabolizowane z wydzieleniem
cyjanowodoru, który jest wysoce toksyczny ponieważ:
Chelatuje jony metali dwu‐ i trójwartościowych w metaloproteinach
np. w cytochromach
Ulega addycji do aldehydów i ketonów z wytworzeniem cyjanohydryn
Reaguje z zasadami Schiffa np. w reakcjach
z wytworzeniem niereaktywnych pochodnych nitryli
transaminacji,
Nitryle służą nie tylko magazynowania azotu, ale przede wszystkim jako
związki toksyczne które mają za zadanie odstraszanie drapieżników
toksyczne,
drapieżników.
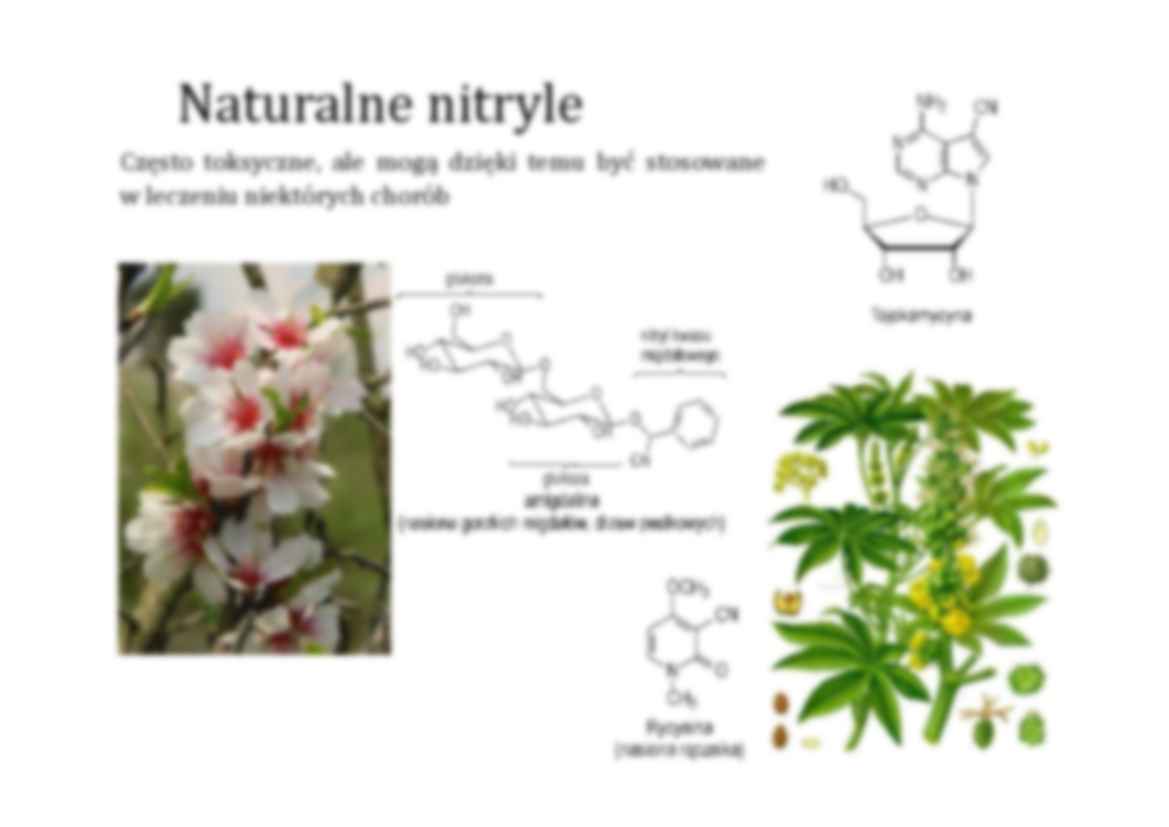
Naturalne nitryle
y
Często toksyczne, ale mogą dzięki temu być stosowane
w leczeniu niektórych chorób
Kierunki hydrolizy nitryli
Nitryle aromatyczne, heterocykliczne i niektóre nienasycone często są
bezpośrednio hydrolizowane do odpowiedniego kwasu przez nitrylazę
(EC 3.5.5.1).
Nitryle alifatyczne są metabolizowane w dwóch etapach – hydrataza nitryli
(EC 4 2 1 84 liaza) przekształca nitryl do odpowiedniego amidu a następnie
4.2.1.84,
amidu,
amidaza (EC 3.5.1.4) hydrolizuje amid do kwasu karboksylowego.
W przypadku hydrolizy optycznie czynnych nitryli, hydratazy nitryli i nitrylazy nie
wykazują najczęściej stereospecyficzności; rozróżnienie enancjomerów następuje
dopiero przy udziale amidazy
Czyste nitrylazy i h d
C
i l
hydratazy nitryli
i li
są przeważnie mało stabilne jako
izolowane
enzymy,
y y
najczęściej
j
j
stosuje się preparaty komórkowe.
Aktywność w kierunku hydrolizy
nitryli
l
musi
być
b ć
najpierw
indukowana.
Nitrylazy
y y
Nitrylazy należą do hydrolaz cysteinowych – nie wymagają kofaktorów, są
inhibowane przez tiole (kwas 5,5’‐ditiobis‐(2‐nitrobenzoesowy)), a mutacja
p
(
,
(
y)),
j
Cys Ala całkowicie niszczy aktywność.
Proponowany mechanizm: rozpad tetraedrycznego produktu pośredniego (Td)
normalnie zachodzi przez wyeliminowanie cząsteczki amoniaku i utworzenie
acylowanego enzymu, a następnie kwasu. Alternatywnie produkt Td może też
rozpaść się z wydzieleniem enzymu (Enz‐Cys‐SH) i wytworzeniem amidu.
Hydratazy nitrylowe (NHazy)
Enzymy z klasy liaz (EC 4.2.1.84) zawierają w centrum aktywnym jony metali:
NHazy żelazowe – niehemowe, zawierające jony żelaza(III): Pseudomonas
chlororaphis B23, Brevibacterium R312, Rhodococcus sp. N‐771
hl
h
b
h d
NHazy kobaltowe – zawierają jony kobaltu(III): Pseudomonas putida NRRL 18668
NHazy zależne jednocześnie od Fe(III) i Co(III): Agrobacterium tumefaciens
Niektóre NHazy wymagają PQQ (pirolochinolinochinon) jako grupy prostetycznej
Znaczenie syntetyczne
Źródłem enzymów hydrolizujących nitryle mogą być mikroorganizmy z rodzaju:
Bacillus, Brevibacterium, Micrococcus, Rhodococcus,
... zobacz całą notatkę






Komentarze użytkowników (0)