To tylko jedna z 9 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


Reakcje charakterystyczne kationów III grupy analitycznej wg Freseniusa kation Co 2+ Położenie kobaltu w szeregu napięciowym: Fe, Co, Ni,...... H
Roztwarzanie kobaltu metalicznego:
Co o + 2H + → Co 2+ + H 2 3Co o + 2NO 3 - + 8H + → 3Co 2+ + 2NO + 4H 2 O
Stężone kwasy siarkowy i azotowy pasywują kobalt
---------------------------------------------------------------------------------------------------------------
Reakcje charakterystyczne:
1) Co 2+ + S 2- ⇔ CoS α przy pH3 CoS α ⇒ CoS β nierozpuszczalny w 1M HCl CoS β + 2H 2 O 2 + 2H + → 3Co 2+ + S 0 + 2H 2 O
3 CoS β H + → 3Co 2+ + 3S 0 + 2NO + 4H 2 O
2) Co 2+ + OH - + NO 3 - ⇔ Co(OH)NO 3 Co 2+ + 2OH - ⇔ Co(OH) 2 Co(OH) 2 + 2OH - ⇔ × 4 Co(OH) 2 + O 2 + 2H 2 O ⇔ 4 Co(OH) 3 w środowisku zasadowym zw. kobaltu(II) utleniają się tlenem z powietrza
3) Co 2+ + 6NH 3 . H 2 O ⇔ [Co(NH 3 ) 6 ] 2+ + 6H 2 O
Co 2+ + NH 3 . H 2 O + NO 3 - ⇔ Co(OH)NO 3 + NH 4 + (może pojawić się też przejściowo osad soli zasadowej)
4[Co(NH 3 ) 6 ] 2+ + O 2 + 2H 2 O ⇔ 4[Co(NH 3 ) 6 ] 3+ + 4OH - 4) Co 2+ + 4SCN - ⇔ [Co(SCN) 4 ] 2- kompleks powstaje w stężonych roztworach SCN - 5) Co 2+ + [Hg(SCN) 4 ] 2- ⇔ Co [ Hg(SCN) 4 ] 6) Co 2+ + 7NO 2 - + 3K + + 2CH 3 COOH ⇔ K 3 [ Co(NO 2 ) 6 ] + NO + 2CH 3 COO - + H 2 O
Reakcje charakterystyczne kationów III grupy analitycznej wg Freseniusa kation Ni 2+ Położenie bizmutu w szeregu napięciowym: Co, Ni, Sn, .... H
Roztwarzanie niklu metalicznego:
Ni o + 2H + → Ni 2+ + H 2 reakcja powolna
3Ni o + 2NO 3 - + 8H + → 3Ni 2+ + 2NO + 4H 2 O
Stężone kwasy siarkowy i azotowy pasywują nikiel
---------------------------------------------------------------------------------------------------------------
Reakcje charakterystyczne:
1) Ni 2+ + S 2- ⇔ NiS α NiS α ⇒ NiS β nierozpuszczalny w 1M HCl
Ni S β + 2H 2 O 2 + 2H + → 3Ni 2+ + S 0 + 2H 2 O
3Ni S β H + → 3Ni 2+ + 3S 0 + 2NO + 4H 2 O
2) Ni 2+ + 2OH - ⇔ Ni(OH) 2 Ni(OH) 2 + 2OH - ⇔ × tlen z powietrza ani woda utleniona nie utleniają Ni(OH) 2 Ni(OH) 2 + ClO - ⇔ NiO 2 + Cl -
(…)
… Cr2+)
Stężone i rozcieńczone kwasy utleniające (np. siarkowy i azotowy) pasywują chrom
---------------------------------------------------------------------------------------------------------------
Reakcje charakterystyczne:
1) Cr3+ + 3S2- + 3H2O ⇔ 2Cr(OH)3 + 3HS- 2) Cr3+ + 3OH- ⇔ Cr(OH)3 pH > 5 Cr(OH)3 + OH- ⇔ [Cr(OH)4]- pH > 11
3) [Cr(OH)4]- ⇔ Cr(OH)3 + OH- przy ogrzaniu proces przebiega…
… Freseniusa
kation Al3+
położenie glinu w szeregu napięciowym: Mg, Al, Zn, ....H
Roztwarzanie glinu metalicznego:
2Alo + 6H+ → 2Al3+ + 3H2 2Alo + 2OH- + 6H2O → 2[Al(OH)4]- + 3H2 Stężone i rozcieńczone kwasy utleniające (np. siarkowy i azotowy) pasywują glin
---------------------------------------------------------------------------------------------------------------
Reakcje charakterystyczne:
1) Al3+ + 3S2…
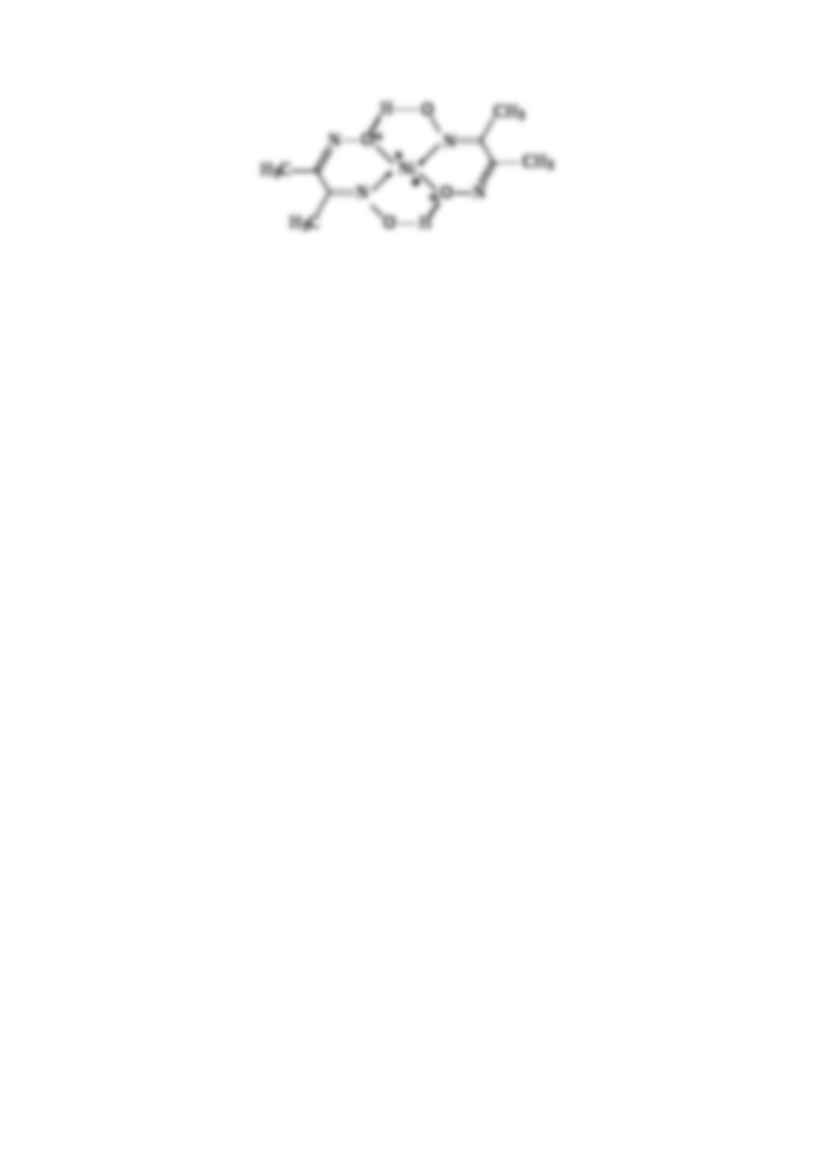
…+ + 2HDMG−Ni(HDMG)2 Reakcje charakterystyczne kationów III grupy analitycznej wg Freseniusa
kationy Fe2+ i Fe3+
Położenie żelaza w szeregu napięciowym: Zn, Fe, Co… H
Roztwarzanie żelaza metalicznego:
Feo + 2H+ → Fe2+ + H2 (w kwasach nieutleniających oraz w rozc. kw. azotowym(V))
Feo + NO3- + 4H+ → Fe3+ + NO + 2H2O
Stężone kwasy siarkowy i azotowy na zimno pasywują żelazo…
… ⇔ Fe(OH)3 + 3NH4+ Fe(OH)3 + NH3.H2O ⇔ ×
4) Fe3+ + CH3COO- ⇔ [Fe(CH3COO)]2+ pH ≈ 7
czerwony kompleks
[Fe(CH3COO)]2+ + 2H2O + 2CH3COO- ⇔ Fe(OH)2CH3COO + 2CH3COOH
5) Fe3+ + K+ + [Fe(CN)6]4- ⇔ KFe[Fe(CN)6] błękit pruski
6) Fe3+ + 6SCN- ⇔ [Fe(SCN)6]3- [Fe(SCN)6]3- + 6F- ⇔ [FeF6]3- + 6SCN- niektóre ligandy rozkładają kompleks rodankowy
7) 2Fe3+ + 2I- ⇔ 2Fe2+ + I2 Reakcje charakterystyczne kationów III grupy analitycznej wg Freseniusa
kation Mn2+
Położenie manganu w szeregu napięciowym: Al, Mn, Zn, ...... H
Roztwarzanie manganu metalicznego:
Mno + 2H+ → Mn2+ + H2 w rozc. kwasach
Mno + SO42- + 4H+ → Mn2+ + SO2 + 2H2O
W stężonym kwasie siarkowym
---------------------------------------------------------------------------------------------------------------
Reakcje charakterystyczne:
1) Mn2+ + S2- ⇔ MnS MnS + 2H…
... zobacz całą notatkę






Komentarze użytkowników (0)