To tylko jedna z 4 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę
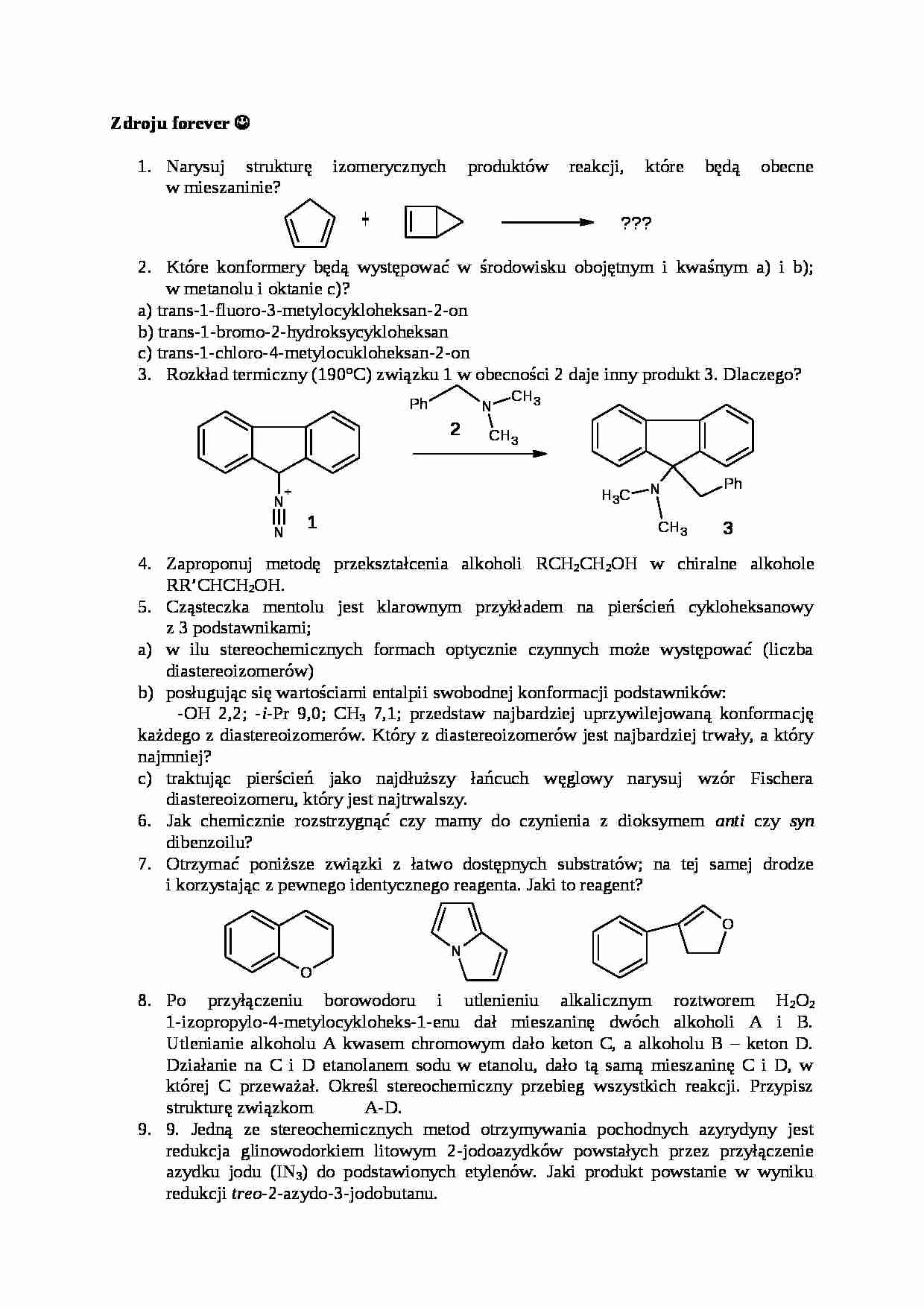


Zdroju forever Narysuj strukturę izomerycznych produktów reakcji, które będą obecne w mieszaninie?
Które konformery będą występować w środowisku obojętnym i kwaśnym a) i b); w metanolu i oktanie c)?
a) trans-1-fluoro-3-metylocykloheksan-2-on
b) trans-1-bromo-2-hydroksycykloheksan
c) trans-1-chloro-4-metylocukloheksan-2-on
Rozkład termiczny (190°C) związku 1 w obecności 2 daje inny produkt 3. Dlaczego?
Zaproponuj metodę przekształcenia alkoholi RCH2CH2OH w chiralne alkohole RR'CHCH2OH.
Cząsteczka mentolu jest klarownym przykładem na pierścień cykloheksanowy z 3 podstawnikami;
w ilu stereochemicznych formach optycznie czynnych może występować (liczba diastereoizomerów)
posługując się wartościami entalpii swobodnej konformacji podstawników:
-OH 2,2; -i-Pr 9,0; CH3 7,1; przedstaw najbardziej uprzywilejowaną konformację każdego z diastereoizomerów. Który z diastereoizomerów jest najbardziej trwały, a który najmniej?
traktując pierścień jako najdłuższy łańcuch węglowy narysuj wzór Fischera diastereoizomeru, który jest najtrwalszy.
Jak chemicznie rozstrzygnąć czy mamy do czynienia z dioksymem anti czy syn dibenzoilu?
Otrzymać poniższe związki z łatwo dostępnych substratów; na tej samej drodze i korzystając z pewnego identycznego reagenta. Jaki to reagent? Po przyłączeniu borowodoru i utlenieniu alkalicznym roztworem H2O2 1-izopropylo-4-metylocykloheks-1-enu dał mieszaninę dwóch alkoholi A i B. Utlenianie alkoholu A kwasem chromowym dało keton C, a alkoholu B - keton D. Działanie na C i D etanolanem sodu w etanolu, dało tą samą mieszaninę C i D, w której C przeważał. Określ stereochemiczny przebieg wszystkich reakcji. Przypisz strukturę związkom A-D.
9. Jedną ze stereochemicznych metod otrzymywania pochodnych azyrydyny jest redukcja glinowodorkiem litowym 2-jodoazydków powstałych przez przyłączenie azydku jodu (IN3) do podstawionych etylenów. Jaki produkt powstanie w wyniku redukcji treo-2-azydo-3-jodobutanu.
Dysponując cykloheksanolem i innymi potrzebnymi Ci reagentami zaproponuj metodę syntezy pochodnej tetracykliny o wzorze:
Zaproponuj prostą metodę syntezy benzo(α)diazepiny z łatwo dostępnych substratów.
Dysponując halogenkami benzylu i etylu i potrzebnymi odczynnikami zaproponuj syntezę stereoselektywną R-2-fenylobutylonitrylu.
Przedstaw możliwość utworzenia monoalkenów, produktów reakcji Zajcewa lub Hoffmana, biegnącej zgodnie z regułą eliminacji E2: R-CH2-CH(X)-CH
(…)
… cykliczny stan przejściowy. Jakich konsekwencji stereochemicznych takiego mechanizmu można oczekiwać dla reakcji Czugajewa przeprowadzonej z: a) użyciem mentolu b) użyciem izomentolu?
Przyłączenie chloru do benzenu daje izomery 1,2,3,4,5,6-haksachlorobenzenu.
ile i jakie?
Czy są wśród nich związki optycznie czynne?
Traktowanie mieszaniny tych związków zasadą w drastycznych warunkach pozostaje tylko 1 izomer, bo reaguje 106 razy wolniej niż inne.
Ustal konfigurację na atomach węgla:
Dysponując (S)-waliną i innymi związkami uzyskaj (R)-serynę o wysokiej czystości.
Treo- i erytro-4-bromo-3-heksanole pod działaniem dymiącego kwasu bromowodorowego dają różne stereoizomeryczne 3,4-dibrooheksany. Z jednego produktu usunięto jeden atom bromu 3 razy szybciej niż z drugiego. Zasugeruj mechanizmy tych reakcji…
…. Wyjaśnij, co odpowiada za taki przebieg reakcji.
Działanie na każdy izomer cis i trans heks-3-enu borowodorem, w którym wszystkie atomy wodoru zastąpiono deuterem i następnie działanie na kompleks borowodoru chloroaminą dało aminy, w których atomy B zastąpiono grupą aminową bez inwersji konfiguracji. Przekształcenie dwóch amin otrzymanych w tych reakcjach w wodorotlenki trietyloaminowe izomerów cis…
... zobacz całą notatkę






Komentarze użytkowników (0)