To tylko jedna z 15 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


Jądro atomowe
1
Czy prawo zachowania masy jest zawsze spełnione ?
Czy jest spełnione na poziomie atomowym ?
• Masa kaŜdego izotopu jest sumą mas protonów,
neutronów i elektronów. Wkład elektronów jest
mało znaczący.
• Masa danego izotopu powinna być (w j.m.a.)
liczbą zbliŜoną do całkowitej
• Izotop 9Be - masa powinna wynosić 9 u,
tymczasem jest niŜsza o 0,0624 u ...
• Czy to błąd rachunkowy ? Jeśli nie, to co się stało
z brakującą masą ?
2
1
„Defekt” masy
• Zgodnie z teorią Einsteina, masa i energia są
równowaŜne E = m·c2
• „Brakująca” masa zamienia się w energię
stabilizacji jądra atomowego, która wynosi w tym
przypadku E = 931,5 MeV = 1,49210-10 J (dla
kaŜdego jądra)
• 1 eV - energia, jaką uzyskuje elektron w polu na
drodze o spadku potencjału o 1 V
• 1 MeV = 106 eV
3
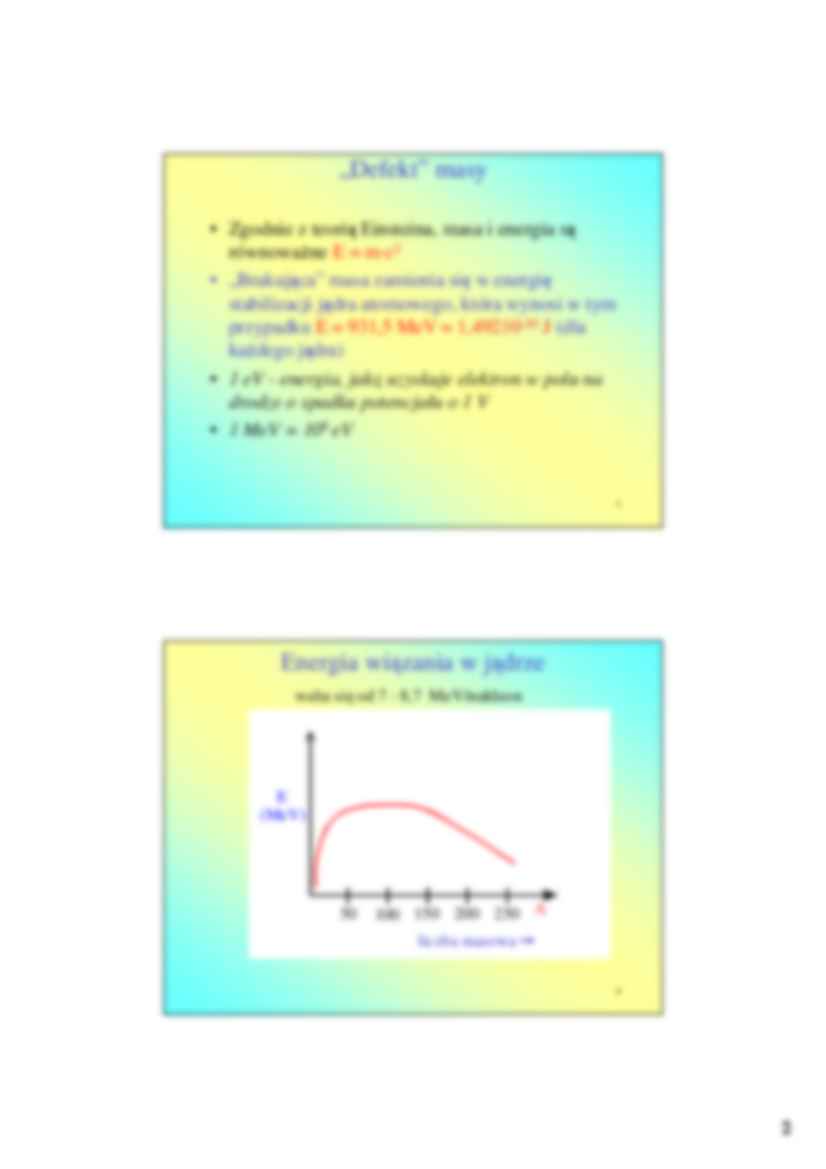
Energia wiązania w jądrze
waha się od 7 - 8,7 MeV/nukleon
E
(MeV)
50
100 150 200 250 A
liczba masowa û
4
2
Stabilność jąder atomowych
160
liczba neutronów w jądrze
140
120
100
80
60
40
20
0
0
20
40
60
liczba atomowa, Z
80
100
5
Promieniotwórczość naturalna
Samorzutny rozpad nietrwałych
nuklidów, połączony z emisją
promieniowania elektromagnetycznego
lub strumienia cząstek
Henri Becquerel, małŜonkowie Curie, 1896
Rodzaje promieniowania:
α
β
γ
- strumień jąder nuklidu izotopu helu
- strumień elektronów
- “twarde” promieniowanie elektromagnetyczne
6
3
Znaczenie promieniotwórczości
Czy badanie promieniotwórczości ma związek z
chemią ?
Tak, dlatego Ŝe:
- promieniotwórczość dostarcza wielu cennych
informacji o budowie jądra atomowego;
- izotopy promieniotwórcze mogą pełnić rolę
“znaczonych” atomów danego pierwiastka i przez to
ułatwiać badanie mechanizmów reakcji chemicznych;
- moŜna zrealizować odwieczne marzenie alchemików,
to znaczy zamieniać jedne pierwiastki w drugie
7
1. Promieniowanie βJest to strumień elektronów, powstających w wyniku
przemiany wewnątrz jądra:
n → p+ + e− + ν
Neutron rozpada się na proton, elektron i antyneutrino
14
6
C → 14 N + e − + ν
7
ogólnie:
A
Z
X → Z+A X'+ β − (e − )
1
8
4
2. Promieniowanie β+
Jest to strumień cząstek o masie elektronów, ale o
ładunku dodatnim, powstających w wyniku przemiany
wewnątrz jądra:
p →n+ e +ν
+
+
Proton rozpada się na neutron, elektron o ładunku
dodatnim (pozyton) i neutrino
A
Z
X → Z −A X ' + β + ( e + )
1
9
3. Promieniowanie α
(emisja cząstki α)
Na skutek przemian węwątrz jądra na zewnątrz
wyrzucany jest strumień cząstek złoŜonych z
dwóch protonów i dwóch neutronów - jąder
izotopu 4 He
2
235
92
A
Z
U → Th + α ( He)
X →
231
90
A− 4
Z− 2
4
2
4
2
X'+ α ( He)
4
2
4
2
10
5
4. Wychwyt K
Jądro pochłania elektron z najbliŜszej
powłoki (K). Wydziela się energia,
związana z przeniesieniem innego elektronu
bliŜej jądra. Elektron łączy się z protonem i
powstaje neutron
p+ + e − → n
A
Z
A
X + e − → Z −1 X '+ energia ( foton )
Wynik - jak dla przemiany β+
11
5. Promieniowanie γ
Przegrupowanie protonów i neutronów w jądrze
prowadzi do wyemitowania
(…)
…
rozszczepialnego
dwa inne jądra
23
Rozszczepienie jąder atomowych
• izotopy rozszczepialne
235
92
U,
239
94
Pu
W czasie rozszczepienia 1 jądra uranu zostaje
wyzwolona energia równa 200 MeV
Rozszczepienie 1 grama uranu wyzwala energię
równą 82·106 kJ (spalenie 2,5 tony węgla!)
24
12
Produkty rozszczepienia
Wydajność
produktów
rozszczepienia
A
80
120
160
25
Rozszczepienie jest reakcją łańcuchową
26
13…
... zobacz całą notatkę






Komentarze użytkowników (0)