To tylko jedna z 7 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę
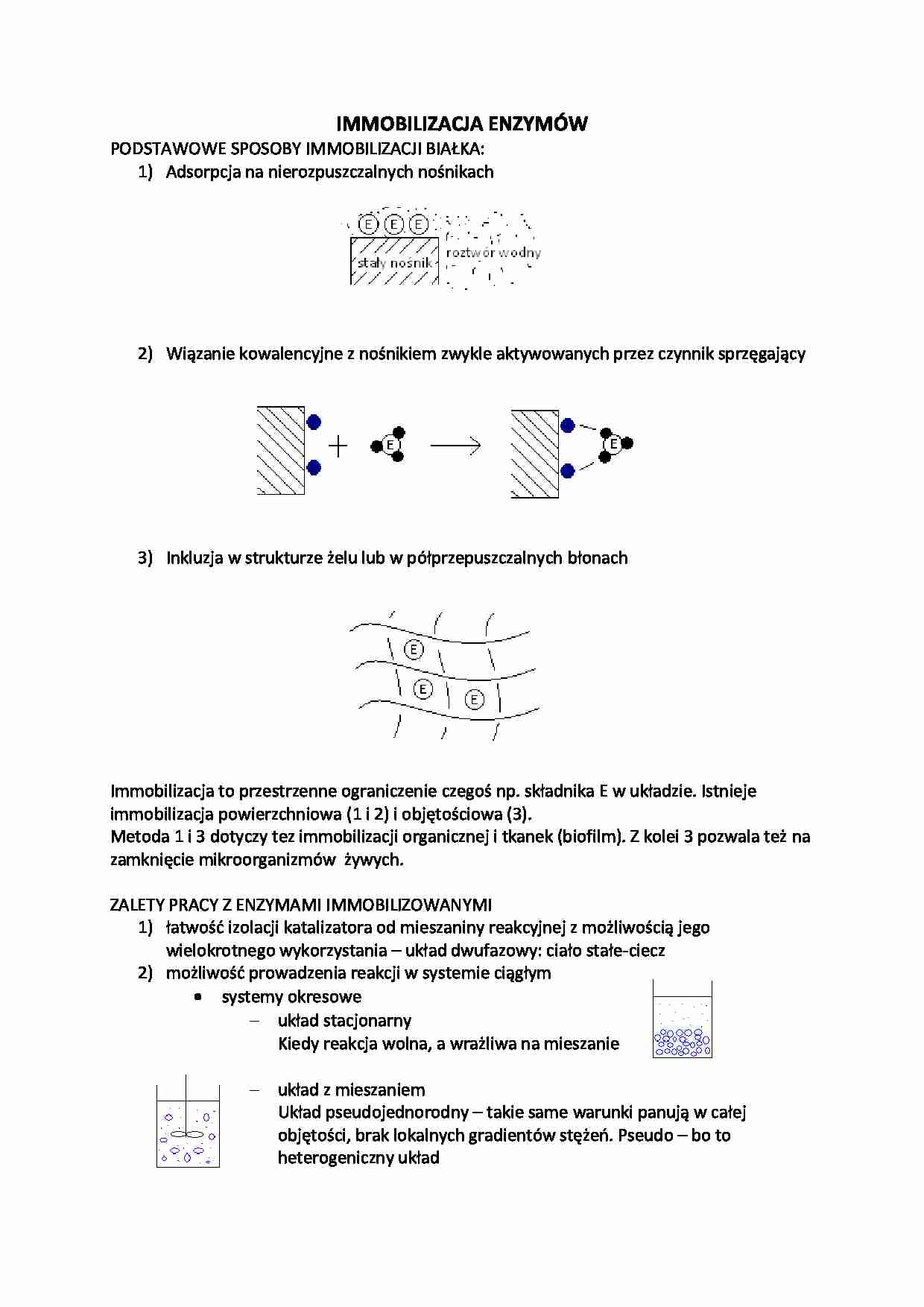


IMMOBILIZACJA ENZYMÓW
PODSTAWOWE SPOSOBY IMMOBILIZACJI BIAŁKA:
Adsorpcja na nierozpuszczalnych nośnikach
Wiązanie kowalencyjne z nośnikiem zwykle aktywowanych przez czynnik sprzęgający
Inkluzja w strukturze żelu lub w półprzepuszczalnych błonach
Immobilizacja to przestrzenne ograniczenie czegoś np. składnika E w układzie. Istnieje immobilizacja powierzchniowa (1 i 2) i objętościowa (3). Metoda 1 i 3 dotyczy tez immobilizacji organicznej i tkanek (biofilm). Z kolei 3 pozwala też na zamknięcie mikroorganizmów żywych.
ZALETY PRACY Z ENZYMAMI IMMOBILIZOWANYMI
łatwość izolacji katalizatora od mieszaniny reakcyjnej z możliwością jego wielokrotnego wykorzystania - układ dwufazowy: ciało stałe-ciecz
możliwość prowadzenia reakcji w systemie ciągłym systemy okresowe
układ stacjonarny
Kiedy reakcja wolna, a wrażliwa na mieszanie układ z mieszaniem Układ pseudojednorodny - takie same warunki panują w całej objętości, brak lokalnych gradientów stężeń. Pseudo - bo to heterogeniczny układ
Proces (pół)ciągły
charakteryzuje się tym, że w sposób ciągły dozujemy do roztwór substratu do bioreaktora (np. kolumna z wypełnieniem)
tam gdzie jest biokatalizator - tam jest reakcja czyli reaktor
żeby był tylko „odbiór produktu” bez substratu należy zmienić (zwiększyć) długość kolumny (czas przebywania w reaktorach) lub natężenie (wolniej dozować)
półciągły, gdy strumień jest dzielony: jest odbiór produktu + zawracanie mieszaniny reakcyjnej
dla E natywnego nie stosuje się procesu ciągłego, bo będzie „wychodził” z kolumny
wysoka stabilność katalizatora zmiana struktury
zmiana specyficzności substratowej białka
ADSORPCJA wiązania wodorowe
oddziaływania van der Waalsa
oddziaływania elektrostatyczne
oddziaływania hydrofobowe
Rzadko nośnikiem jest Caktywny, raczej polimer akrylowy, tworzywa sztuczne, granit czy szkło.
(…)
…
ADSORPCJA wiązania wodorowe
oddziaływania van der Waalsa
oddziaływania elektrostatyczne
oddziaływania hydrofobowe
Rzadko nośnikiem jest Caktywny, raczej polimer akrylowy, tworzywa sztuczne, granit czy szkło.
Silny wpływ środowiska
wartość pH, siła jonowa roztworu białka (oddziaływanie elektrostatyczne)
stężenie enzymu w roztworze (liczba miejsc wiązania enzymu)
temperatura (dyfuzja T, aktywność enzymu T )
Powierzchnia właściwa, porowatość nośnika (średnica porów. ½ średnica białka)
Adsorpcja
duża dostępność do czyszczenia (-)uwzględnia niską trwałość,
nośników (-) enzymu (+) silny wpływ środowiska(pH), odrywanie się nośnika (desorpcja)
Nośniki:
Nieorganiczne:
krzemionka
wodorotlenek glinu/tytanu
glinokrzemiany
szkło porowate
węgiel aktywny
materiały ceramiczne
Organiczne:
polisacharydy (agar, celuloza, skrobia…
….
ZAMKNIĘCIE WE WŁÓKNACH
Roztwór enzymu w organicznym roztworze monomeru, który polimeryzując tworzy włókno pochodne celulozy, polichlorek winylu, poli-L-metyloglutaminian
Dysze przytłaczające roztwór do cieczy organicznych (np. toluen), w której następuje polimeryzacja.
Rola kopolimeru:
wiązanie pośrednie z monomerami
stwarza środowisko, które ułatwia łączenie się z monomerami
SIECIOWANIE np. aldehyd…
…-
IMMOBILIZACJA NA DRODZE CHEMICZNEJ
duża trwałość, mały wpływ środowiska zewnętrznego (+)
oddalenie enzymu od nośnika (-), zmniejszenie wpływu dyfuzji (substratu)
zmiana właściwości immobilizowanego katalizatora (+/-)
INKLUZJA W ŻELU/BŁONACH PÓŁPRZEPUSZCZALNYCH
monomer polimer
Efektywność immobilizacji na drodze inkluzji
zawartość enzymu charakter polimerycznej matrycy
w żelu (+kopolimer)
rozmiary porów w żelu…
... zobacz całą notatkę






Komentarze użytkowników (0)