To tylko jedna z 18 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


Całkowanie równań kinetycznych
Przygotował: Kamil Paduszyński
© 2010
(c) Kamil Paduszyński 2010
1
PROBLEM
Rozważamy reakcję chemiczną, np. A + 2B = C
Pytania:
● Jakie jest równanie kinetyczne dla tej reakcji?
● Jak całkować równanie kinetyczne?
● Jaki jest rząd tej reakcji?
● Jaka jest wartość stałej szybkości dla tej reakcji?
UWAGA! Wszelkie algorytmy prezentuję tylko dla stężeń molowych.
Korzystanie z nich dla układów, w których dostępne są inne parametry
(w szczególności ciśnienie) zostawiam do samodzielnego nauczenia się.
(c) Kamil Paduszyński 2010
2
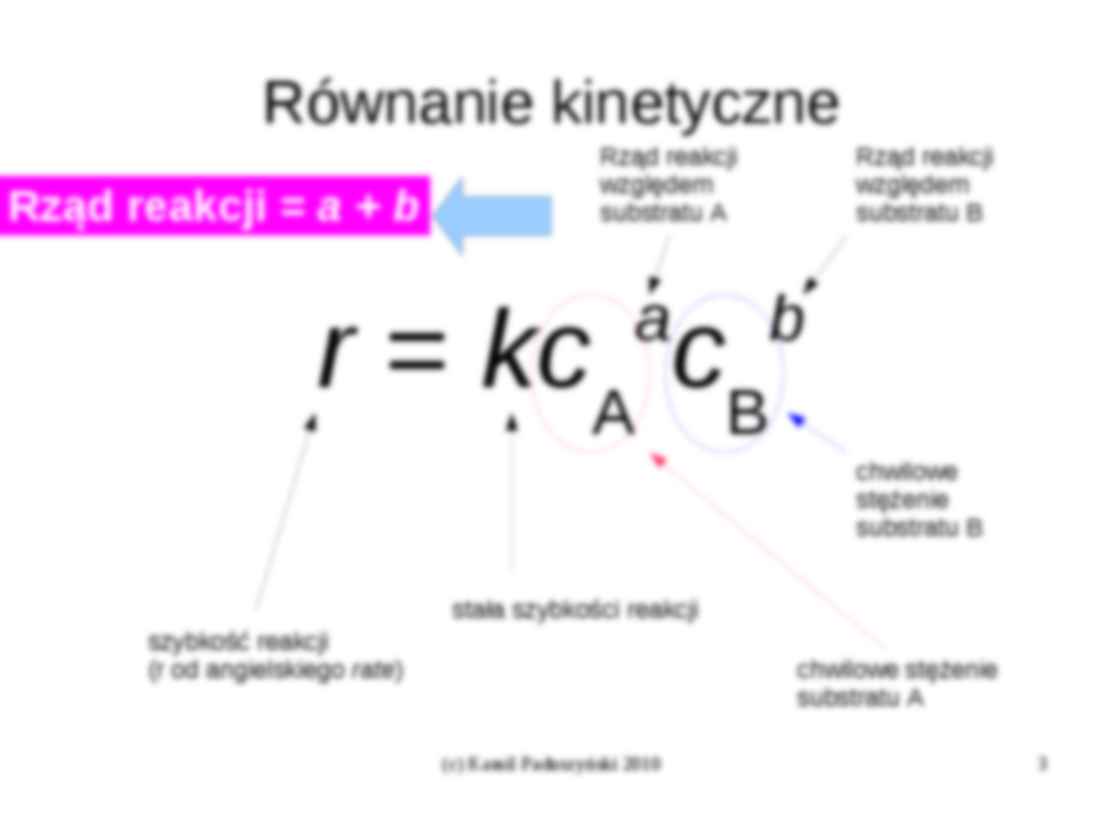
Równanie kinetyczne
Rząd reakcji = a + b
Rząd reakcji
względem
substratu A
Rząd reakcji
względem
substratu B
a
b
A B
r = kc c
chwilowe
stężenie
substratu B
stała szybkości reakcji
szybkość reakcji
(r od angielskiego rate)
chwilowe stężenie
substratu A
(c) Kamil Paduszyński 2010
3
KOMENTARZE
W równaniu kinetycznym występują tylko
chwilowe stężenia substratów (przy najmniej
w przypadkach, które analizować będziemy w
pierwszej kolejności; niedługo uciekniemy od
tego założenia)
Rząd reakcji jest SUMĄ wykładników
stojących przy chwilowych
stężeniach poszczególnych
substratów.
A a co chodzi z szybkością reakcji r?
r=
Szybkość reakcji to znormalizowana
(współczynnikiem równania reakcji)
Czasowa pochodna stężenia molowego
reagenta(substratu lub produktu) (c) Kamil Paduszyński 2010
1
dcR
υR
dt
4
Całkowanie równania kinetycznego
Zaliczenie ćwiczeń
Równanie kinetyczne: po co to?
Równanie kinetyczne podaje nam zależność stężenia
każdego z reagentów w funkcji czasu. Chwilowe stężenia są
właśnie funkcjami czasu. Funkcje są więc tutaj
niewiadomymi, bo ich znajdowaniem zajmuje się kinetyka.
Wobec tego równanie kinetyczne jest równaniem, w którym
niewiadomą jest funkcja. A jak się takie równania nazywają?
A no równaniami różniczkowymi...
Rząd reakcji
Stała szybkości
Równanie kinetyczne to równanie różniczkowe,
którego rozwiązaniem są zależności czasowe
stężeń wszystkich reagentów.
Po co rozwiązywać
równanie
kinetyczne?
Notabene: rozwiązywanie równania
różniczkowego nazywa się zwykle 5
(c) Kamil Paduszyński 2010
całkowaniem.
Całkowanie równania kinetycznego
Wymagam od Państwa umiejętności całkowania (razem z
wyprowadzeniem – odpowiedzi gotowe nie będą nawet
sprawdzane!) następujących równań kinetycznych:
r = kcA
1
a
(odpowiada reakcji A = produkty, r = -dcA/dt)
a
r = kcA c
b
B
2
(odpowiada reakcji A + B = produkty, r = -dcA/dt = -dcB/dt)
Dwa przypadki: 1) stężenia początkowe obu substratów takie
same (ławte); 2) stężenia początkowe obu substratów różne
(wprowadzenia „ubytku stężenia”; trudniejsze)
(c) Kamil Paduszyński 2010
6
Równanie
1
Rząd reakcji (mamy dany lub jest
do wyznaczenia, np. metodą
całkowo-graficzną).
r=
1
dcA
υA
dt
= kc
a
A
Warunek początkowy: cA(0) = cA0
Rozwiążmy najpierw przypadek a = 2010
(c) Kamil Paduszyński 1...
Stężenie początkowe
7
substratu A (na ogół znane)
Równanie
cA
∫
cA0
1
1
dcA
υA cA
a=1
t
= ∫ kdt
0
„czary mary”
... zobacz całą notatkę






Komentarze użytkowników (0)