To tylko jedna z 11 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę
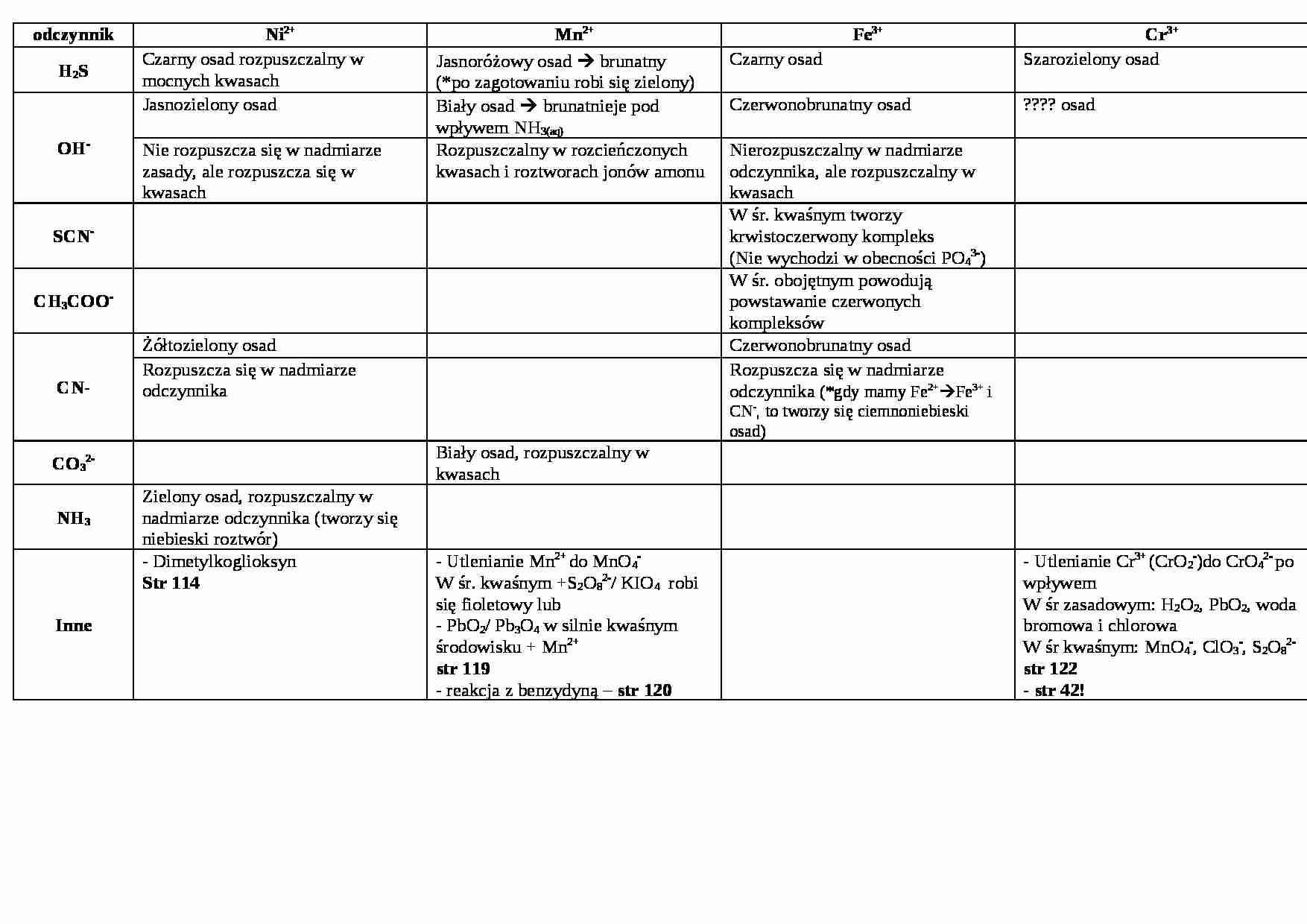


odczynnik
Ni2+
Mn2+
Fe3+
Cr3+
H2S
Czarny osad rozpuszczalny w mocnych kwasach
Jasnoróżowy osad brunatny
(*po zagotowaniu robi się zielony)
Czarny osad
Szarozielony osad
OH-
Jasnozielony osad
Biały osad brunatnieje pod wpływem NH3(aq)
Czerwonobrunatny osad
???? osad
Nie rozpuszcza się w nadmiarze zasady, ale rozpuszcza się w kwasach
Rozpuszczalny w rozcieńczonych kwasach i roztworach jonów amonu
Nierozpuszczalny w nadmiarze odczynnika, ale rozpuszczalny w kwasach
SCN-
W śr. kwaśnym tworzy krwistoczerwony kompleks
(Nie wychodzi w obecności PO43-)
CH3COO-
W śr. obojętnym powodują powstawanie czerwonych kompleksów
CN-
Żółtozielony osad
Czerwonobrunatny osad
Rozpuszcza się w nadmiarze odczynnika
Rozpuszcza się w nadmiarze odczynnika (*gdy mamy Fe2+Fe3+ i CN-, to tworzy się ciemnoniebieski osad)
CO32-
Biały osad, rozpuszczalny w kwasach
NH3
Zielony osad, rozpuszczalny w nadmiarze odczynnika (tworzy się niebieski roztwór)
Inne
- Dimetylkoglioksyn
Str 114
- Utlenianie Mn2+ do MnO4-
W śr. kwaśnym +S2O82-/ KIO4 robi się fioletowy lub
- PbO2/ Pb3O4 w silnie kwaśnym środowisku + Mn2+
str 119
- reakcja z benzydyną - str 120
- Utlenianie Cr3+ (CrO2-)do CrO42-po wpływem W śr zasadowym: H2O2, PbO2, woda bromowa i chlorowa
W śr kwaśnym: MnO4-, ClO3-, S2O82-str 122
- str 42!
... zobacz całą notatkę






Komentarze użytkowników (0)