To tylko jedna z 16 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę
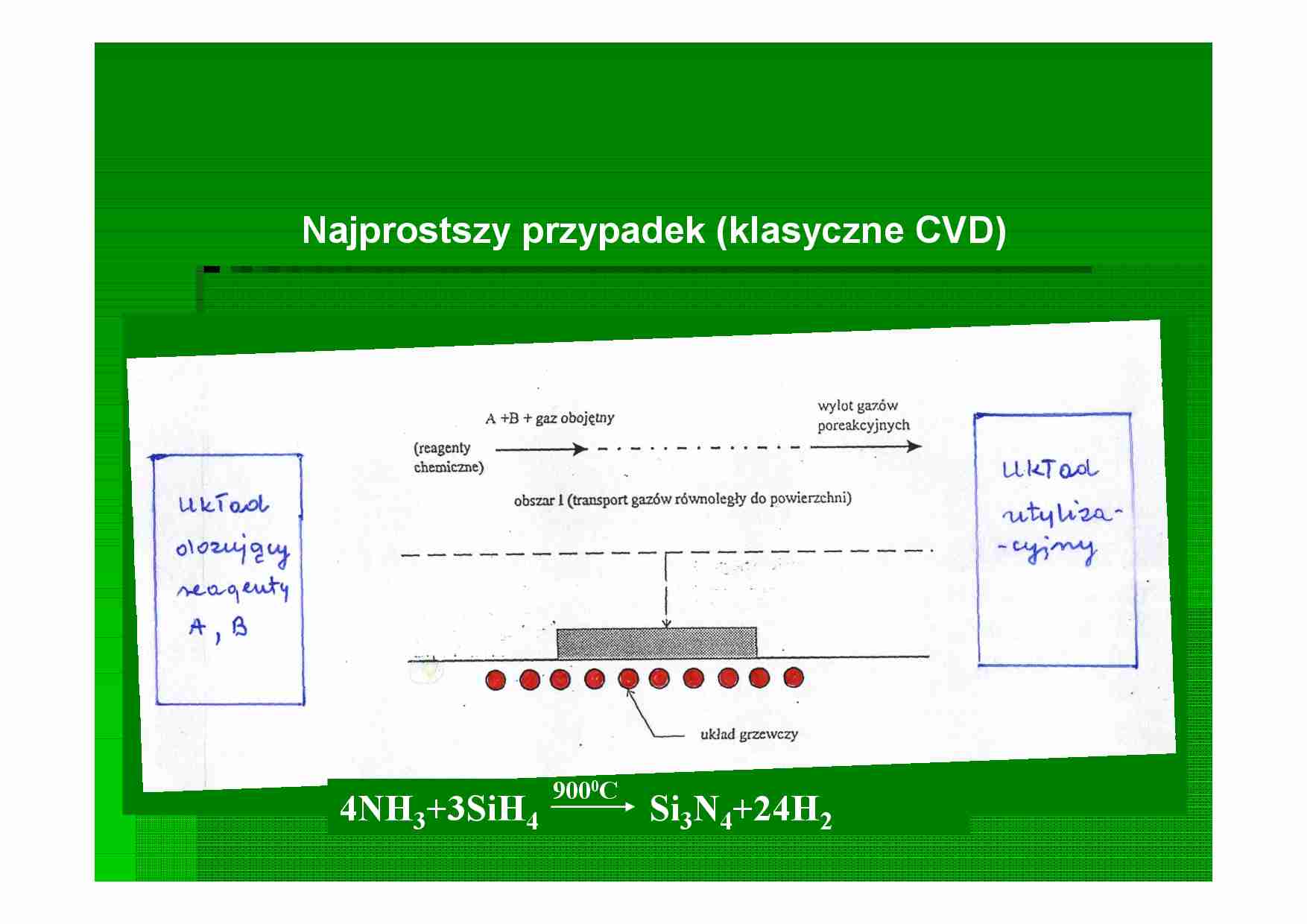

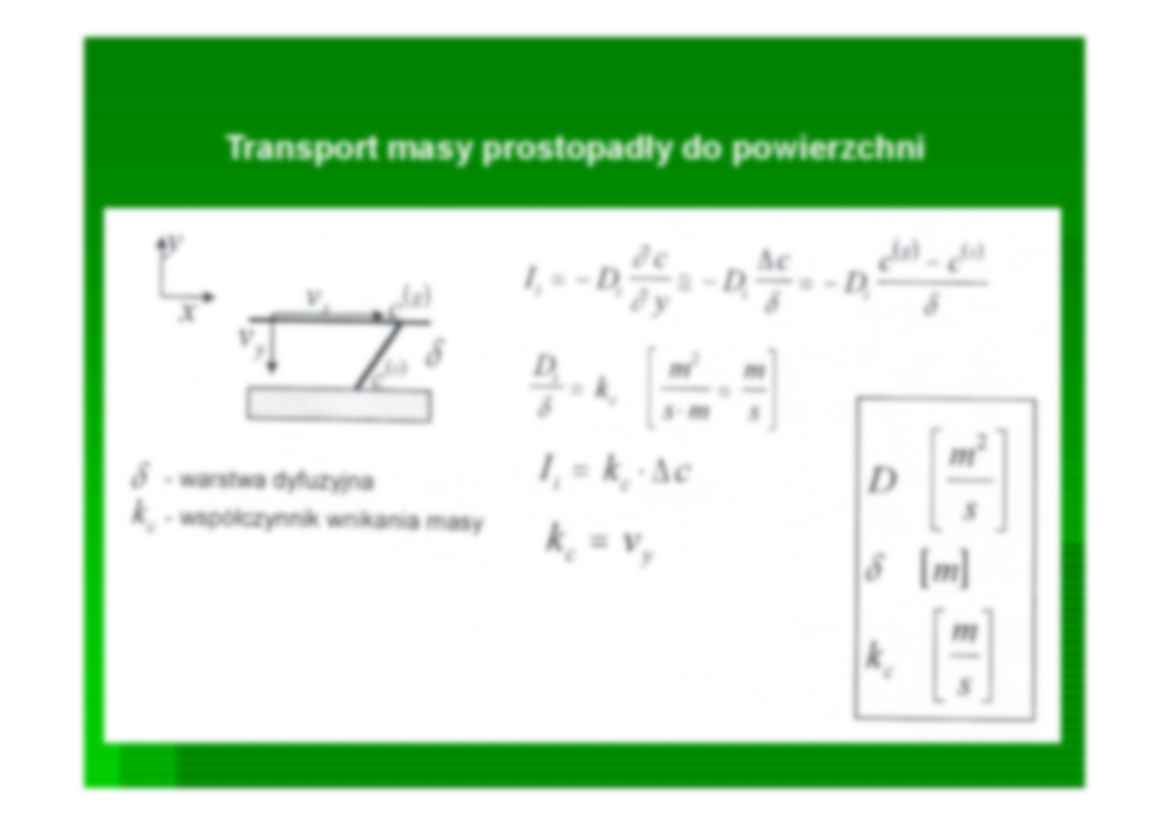
Najprostszy przypadek (klasyczne CVD) 4NH 3+3SiH4 Si 3N4+24H2 9000C Transport masy równoległy do powierzchni Przepływ laminarny Tory molekuł są prostoliniowe, równoległe do osi rury (przewodu) Rozkład prędkości Transport masy prostopadły do powierzchni DYFUZJA W GAZACH – molekularne przenoszenie masy Określenie wartości współczynnika dyfuzji Opis doświadczalny – I prawa Ficka Teoretyczne określenie wsp. dyfuzji w oparciu o uproszczoną teorie kinetyczną gazów Z: gaz składa się z dwu cząsteczek A i B rozróżnialnych lecz o tej samej masie i średnicy (izotopy) B=A Równanie na współczynnik samodyfuzji DLA GAZÓW DOSKONAŁYCH Dla gazu A+B d A≠dB mA≠mB Określanie wielkości gradientu c(s) możliwe do określenia w przypadku gdy układ znajduje się w równowadze termodynamicznej x c D i i v c x c D N i i i v c i - człon dyfuzyjny - człon konwekcyjny Wektor strumienia masy Warstwy w procesie CVD powstają na zasadzie: Warstwy w procesie CVD powstają na zasadzie Gazowe reagenty= Gazowe reagenty= stały stały materiał materia gazowy gazowy produkt produk + MECHANIZM REAKCJI W FAZIE GAZOWEJ I II III IV Adsorpcja SiCl 4 (Si-C-H 3 *) (s)+Cl3SiCl (Si-C-Si-Cl*) (s)+3HCl(g) Adsorpcja CH 4 na powierzchni obsadzonej Si (Si-Cl*) (s)+HCH3 (Si-C-H 3 *) + HCl (g) CH 4, SiCl4, HCl CH 3SiCl4 + HCl = CH4 + SiCl4 METODY OKREŚLANIA RÓWNOWAGI FAZY GAZOWEJ WZGLĘDEM POWIERZCHNI TEORETYCZNE a) obliczenia termodynamiczne (ΔG) (układ w równowadze) b) metoda izoterm Langmuira c) metoda oparta na teorii stanu przejściowego d) eksperymentalne PROCESY CHEMICZNE W UKŁADZIE CVD Określenie równowagi powierzchni z fazą gazową Ujęcie oparte na izotermach Langmuira W ujęciu kinet. teorii gazów N – lb.Avogadro; σ 0 – powierzchnia zajmowana przez cząsteczkę adsorbatu; τ0 – czas przebywania cząst. w węźle na powierzchni; R – stała gazowa; T – temperatura; m – masa cząsteczkowa; ε – energia adsorpcji METODA OPARTA NA TEORII STANU PRZEJŚCIOWEGO Badania struktury przy użyciu spektoskopii w podczerwieni
... zobacz całą notatkę






Komentarze użytkowników (0)