To tylko jedna z 3 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę
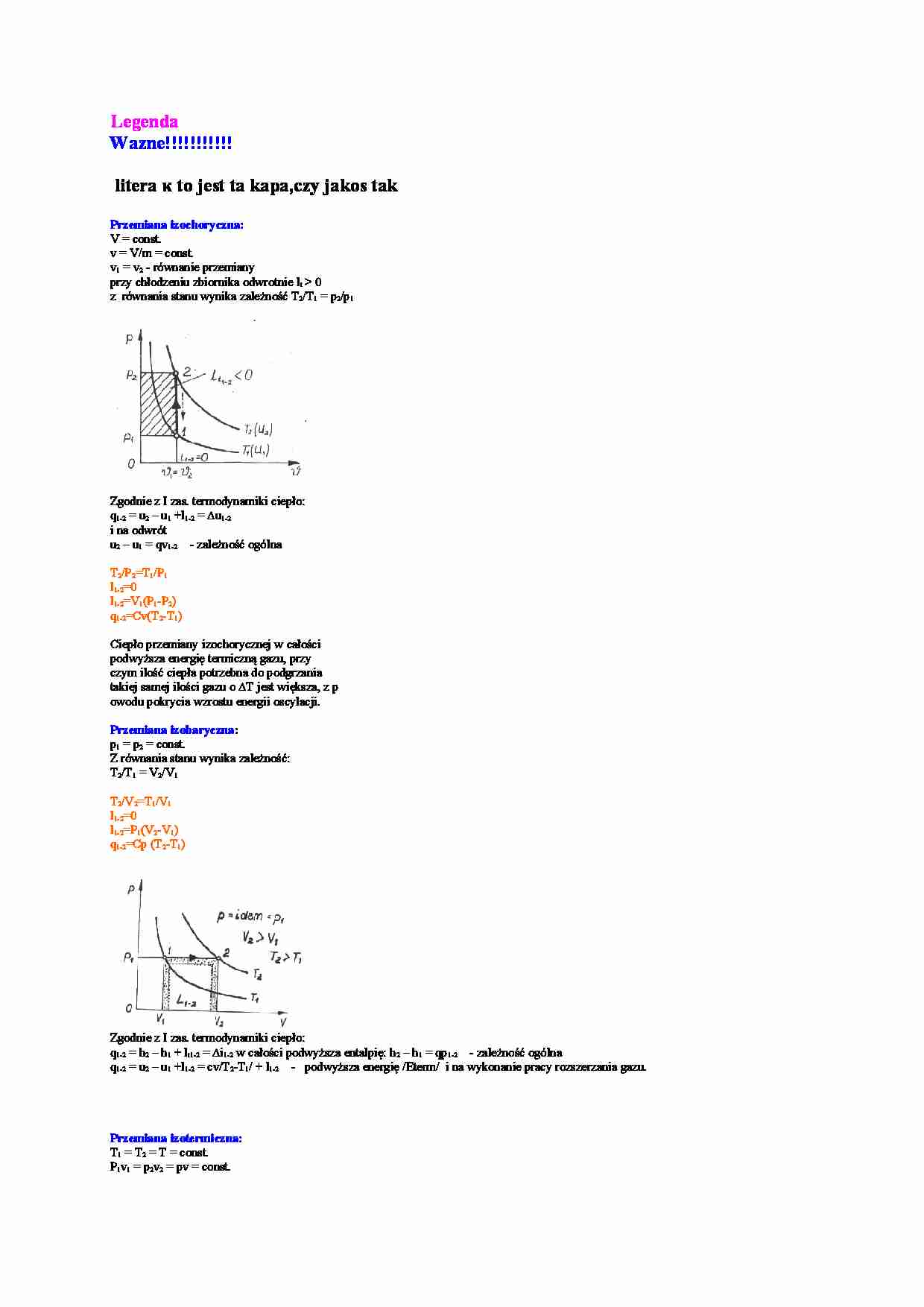


Legenda Wazne!!!!!!!!!!! litera κ to jest ta kapa,czy jakos tak Przemiana izochoryczna: V = const. v = V/m = const. v1 = v2 - równanie przemiany przy chłodzeniu zbiornika odwrotnie lt 0 z równania stanu wynika zależność T2/T1 = p2/p1 Zgodnie z I zas. termodynamiki ciepło: q1-2 = u2 – u1 +l1-2 = ∆u1-2 i na odwrót u2 – u1 = qv1-2 - zależność ogólna T2/P2=T1/P1 l1-2=0 l1-2=V1(P1-P2) q1-2=Cv(T2-T1) Ciepło przemiany izochorycznej w całości podwyższa energię termiczną gazu, przy czym ilość ciepła potrzebna do podgrzania takiej samej ilości gazu o ∆T jest większa, z p owodu pokrycia wzrostu energii oscylacji. Przemiana izobaryczna: p1 = p2 = const. Z równania stanu wynika zależność: T2/T1 = V2/V1 T2/V2=T1/V1 l1-2=0 l1-2=P1(V2-V1) q1-2=Cp (T2-T1) Zgodnie z I zas. termodynamiki ciepło: q1-2 = h2 – h1 + lt1-2 = ∆i1-2 w całości podwyższa entalpię: h2 – h1 = qp1-2 - zależność ogólna q1-2 = u2 – u1 +l1-2 = cv/T2-T1/ + l1-2 - podwyższa energię /Eterm/ i na wykonanie pracy rozszerzania gazu. Przemiana izotermiczna: T1 = T2 = T = const. P1v1 = p2v2 = pv = const. Ciepło właściwe przemiany: Ct = Q / m * ∆T → ∞ Korzystając z I zas. termodynamiki obliczamy: q1-2 = u2 – u1 + l1-2 = cv/T2 – T1/ + l1-2 = l1-2 q1-2 = h2 – h1 + lt1-2 = cp/T2 – T1/ + lt1-2 = lt1-2 zatem l1-2 = lt1-2 = q1-2 ( = p1v1 * ln(v2/v1) = p1v1 * ln(p1/p2) ( = RT1 * ln(v2/v1) = RT1 * ln(p1/p2) Czyli doprowadzone ciepło : Q1-2 = L1-2 = Lt1-2 W całości idzie na wykonanie pracy. Eterm. gazu nie ulega zmianie. P2/P1=V1/V2 l1-2=lt1-2=q1-2=P1v1ln(P1/P2)=P1v1ln(v2/v1)=RT1ln(P1/P2) Przemiana adiabatyczna Q1-2=q1-2=dq=0 Z I zas.termodynamiki otrzymujemy: a) Q1-2=0=U2-U1+L1-2 L1-2=U1-U2 /m l1-2=u1-u2 kosztem u b) Q=0=H2-H1+Lt1-2 Lt1-2=H1-H2 /m lt1-2=h1-h2 kosztem h Równanie przemiany Przesunięcie dx-dv Cp/Cv=κ rown.Poissona p1v1κ=p2v2κ=pvκ=const- Zaleznosci miedzy parametrami p2/p1=(v1/v2)κ v2/v1=(p1/p2)1/κ T2/T1=(V1/V2)κ-1 T2/T1=(p2/p1)κ-1/κ PRACA ABSOLUTNA l1-2=RT1/κ-1[1-(p2/p1)κ-1/ κ] PRACA TECHNICZNA lt1-2l1-2 c=Q/m∆T=0 cieplo właściwe przemiany l1-2=Cv(T1-T2) lt1-2=Cp(T1-T2) q1-2=0 κ=Cp/Cv Cp= (κ/κ-1)R Cv=(1/ κ-1)R Cv=Cp-R Przemiana politropowa c=Q/m∆T=0 a wiec ogolna przemiana Rownanie przemiany p1v1n=p2v2n=pvn=const Wykladnik politropy n=C-Cp/C-Cv Zależności pomiedzy parametrami p2/p1=(v1/v2)n v2/v1=(p1/p2)1/n T2/T1=(V1/V2)n-1 T2/T1=(p2/p1)n-1/n Cieplo wlasciwe n=C-Cp/C-Cv c=(n – κ / n – 1) Cv gdy n→1 c→∞ (nieokreślone) pv1=const
... zobacz całą notatkę






Komentarze użytkowników (0)