To tylko jedna z 3 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


Stany skupienia gazowy (H, He, N,O,F,Ne,Cl,Ar, pozostałe helowce)
ciekły (Br,Hg + Ga,Cs,Fr posiadają temp. topnienia od +27 do 30 st C)
ciało stałe - reszta pierwiastków
Promieniotwórczość naturalna - pierwiastki ciężkie (od Z = 84 do Z = 92) występują WYŁĄCZNIE w postaci izotopów promieniotwórczych. izotopy te tworzą 3 szeregi promieniotwórcze:
4n Torowy 232Th - 208Pb
4n+2 Uranowo-radowy 238U - 206Pb
4n+3 Uranowo-aktynowy 235U - 207Pb
- izotopy promieniotwórcze o Z92
- sztuczne izotopy promieniotwórcze pierwiastków o Z A+ + e
A+ + energia (2) - A2+ + e
A2+ + energia (3) - A3+ + e
energia (1) 2,1
Stopnie utlenienia pierwiastków grup głównych
Maksymalny stopień utlenienia zazwyczaj (za wyjątkiem wyjątków) pokrywa się z numerem grupy głównej . Wraz ze wzrostem nr grupy wzrasta kwasowość, wraz ze spadkiem numeru grupy wzrasta zasadowość.
(…)
… -> 206Pb
4n+3 Uranowo-aktynowy 235U -> 207Pb
- izotopy promieniotwórcze o Z<84 sztuczna
- Tc (Z=43), Pm (Z=61), At (Z=85)
- pierwiastki o Z>92
- sztuczne izotopy promieniotwórcze pierwiastków o Z<92
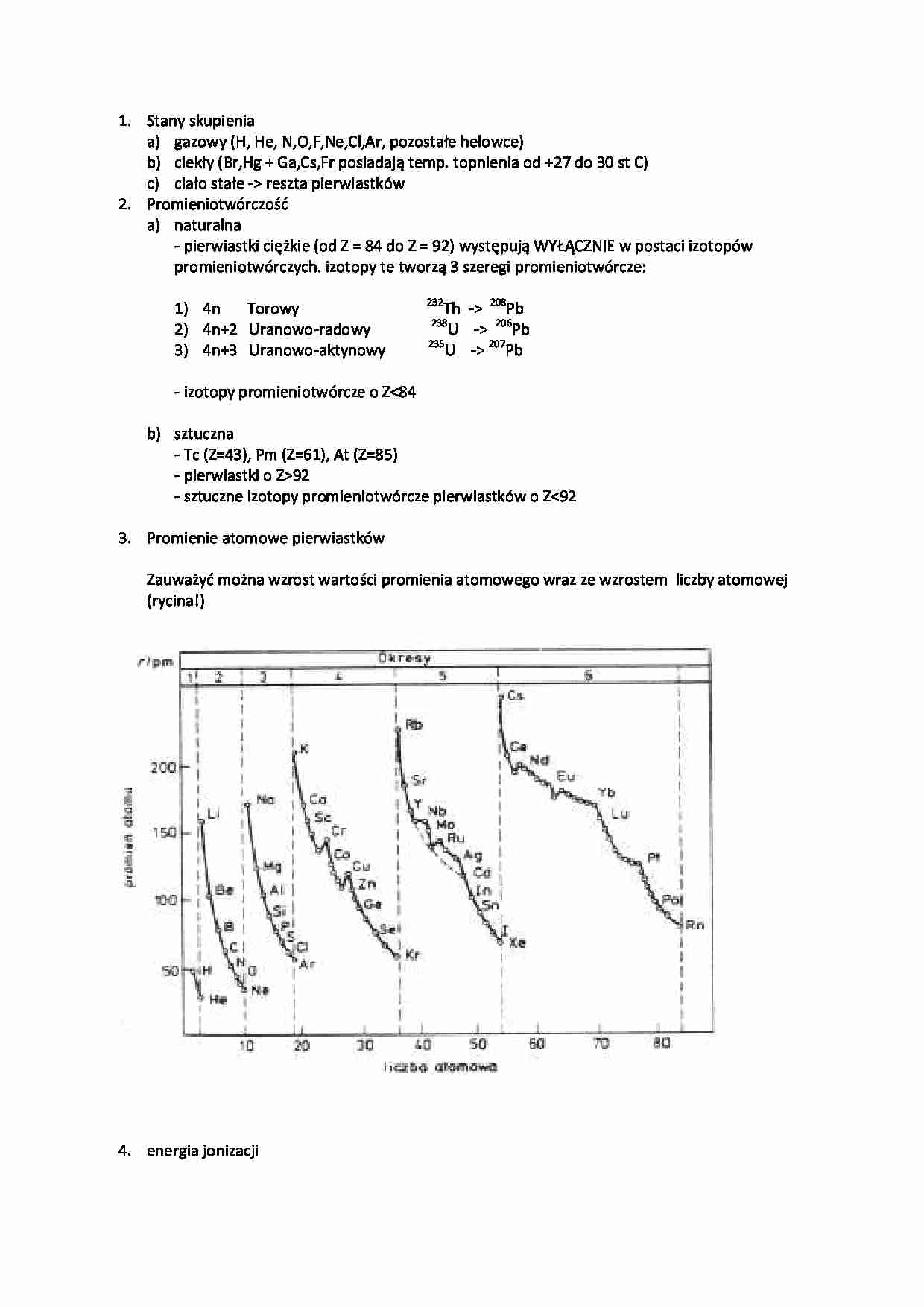
Promienie atomowe pierwiastków
Zauważyć można wzrost wartości promienia atomowego wraz ze wzrostem liczby atomowej (rycina!) energia jonizacji jest to energia potrzebna do oderwania elektronu z atomu…
… zmian jw. dla wybranych pierwiastków ma wartości ( w kJ/mol):
Fluor -344
Chlor -349
Brom -329
Wodór -72
Elektroujemność
Umowna miara skłonności atomu do przyciągania elektronów podczas tworzenia wiązania chemicznego. Jest kilka skal : Paulinga, Mullikana, Allreda i Rochowa. Najczęściej (w sumie prawie zawsze) stosowana jest elektroujemność wg Paulinga. Trendy w zakresie zmian jak w powinowactwie i energii jonizacji. metale wykazują elektroujemność < 1,8
półmetale 1,8 - 2,1 za wyjątkiem selenu
niemetale >2,1
Stopnie utlenienia pierwiastków grup głównych
Maksymalny stopień utlenienia zazwyczaj (za wyjątkiem wyjątków) pokrywa się z numerem grupy głównej . Wraz ze wzrostem nr grupy wzrasta kwasowość, wraz ze spadkiem numeru grupy wzrasta zasadowość. Charakter chemiczny tlenków Pola jasne - tlenki…
... zobacz całą notatkę






Komentarze użytkowników (0)