To tylko jedna z 4 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


Temat: Liczba Avogadro
1. Wstęp
Liczba cząsteczek zawartych w jednym molu dowolnej substancji, zwana jest liczbą Avogadro i oznaczana symbolem NA. Za najdokładniejszą wartość liczby Avogadro przyjmuje się obecnie:
NA = 6.022045 (31) . 1023 mol-1 Znajomość liczby Avogadro pozwala na obliczenie bezwzględnej masy atomu i cząsteczki. Np. w 1 molu atomów wodoru, tj. w 1.0079 g wodoru, mamy 6.022045 . 1023 atomów wodoru. Masa pojedynczego atomu wodoru, mH, wynosi więc:
Jeżeli weźmiemy pod uwagę dwie różne substancje gazowe (każda w ilości 1 mol) to zawierają one taką samą liczbę cząsteczek. Zgodnie z hipotezą Avogadro muszą więc mieć taką samą objętość jeżeli wykazują taką samą temperaturę (T) i takie samo ciśnienie (p). Zatem w danych warunkach (p i T) objętość 1 mola cząsteczek dowolnej substancji gazowej jest stała1. W warunkach normalnych (T = 273.15 K, p = 101325 Pa) objętość ta wynosi 22.41383 (70) dm3. mol-1.
Stała Avogadro, NA, może być wyznaczona na drodze eksperymentalnej różnymi metodami. Jedną z najprostszych jest elektroliza H2O. W trakcie procesu elektrolizy, w wyniku rozkładu H2O, na katodzie wydziela się gazowy wodór a na anodzie tlen. Reakcje elektrodowe opisano poniżej:
K: (1)
A: (2)
Rejestrując wartość natężenia prądu elektrolizy I oraz wyznaczając objętość wydzielonego gazu V (np. H2) można obliczyć stałą NA.
2. Cel ćwiczenia
Wyznaczyć wartość liczby Avogadro.
Odczynniki, materiały i aparatura:
Roztwory bazowe: 1 M NaOH w H2O
Elementy układu pomiarowego: Reaktor (naczynie szklane z pokrywką)
Dwie strzykawki Amperomierz
Zasilacz elektrolizera
Termometr
Elektrody (izolowane druciki) 3. Wykonanie
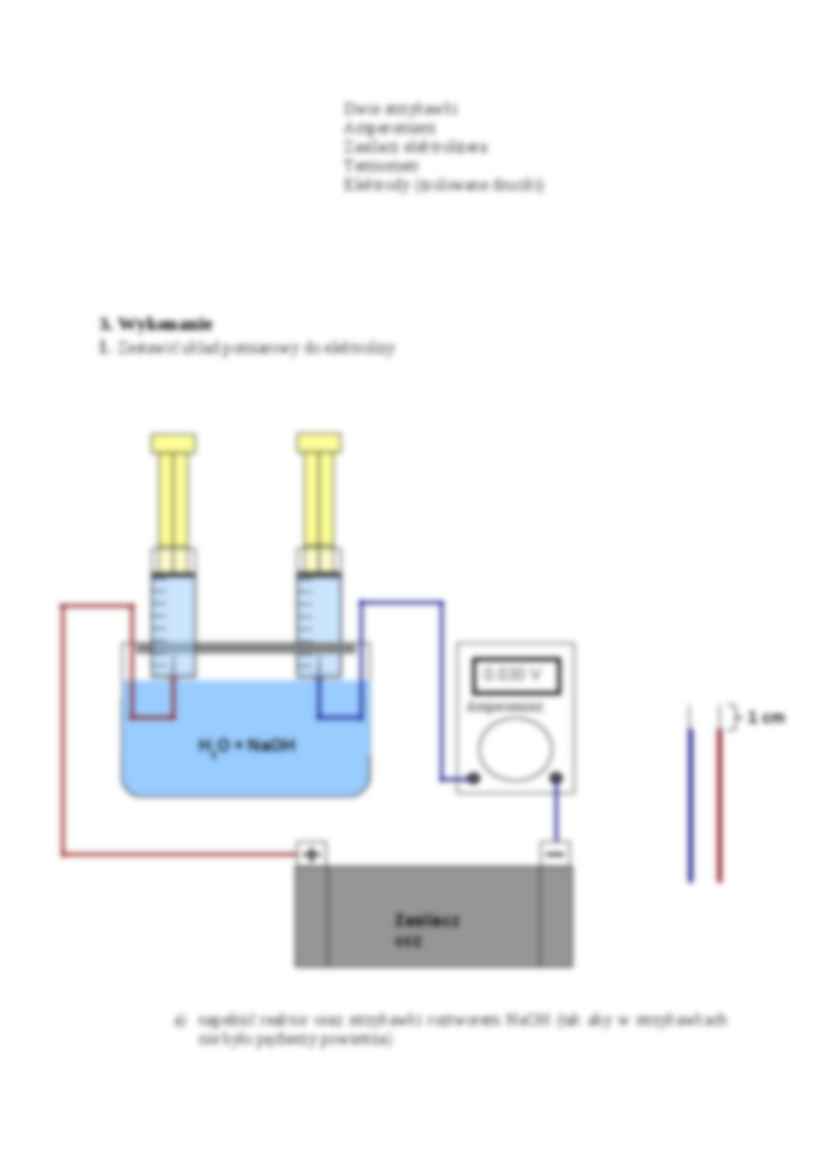
1. Zestawić układ pomiarowy do elektrolizy napełnić reaktor oraz strzykawki roztworem NaOH (tak aby w strzykawkach nie było pęcherzy powietrza) strzykawki umieścić w otworach pokrywki w taki sposób aby po nakryciu elektrolizera ich końcówki zanurzone były w elektrolicie
poprzez otwory w każdej ze strzykawek włożyć elektrody do przestrzeni elektrodowych (końcówka elektrody powinna być widoczna w strzykawce)
elementy zestawu pomiarowego (zasilacz, amperomierz, elektrody) połączyć ze sobą szeregowo w obwód elektryczny
(…)
…
2,33
2,38
2,20
2,40
2,16
2,38
3,01
3,07
2,12
4,79∙1023
5. Obliczanie ilości moli wydzielonego wodoru na podstawie równania stanu gazu doskonałego.
pV = nRT
p — ciśnienie; p = 760 mm Hg = 101325 [Pa]
V — objętość; =1,0 cm3 = 0,000001 [m3]
T — temperatura; T = 210C = 294 [K]
R — stała gazowa; R = 8,31 n- ilość moli wydzielonego wodoru
6.Oblicznie liczby moli elektronów jaka przepłynęła przez badany…
…, że rozpatrywane substancje gazowe traktowane są jak gaz doskonały i stosują się do praw gazu doskonałego.
H2O + NaOH
0.030 V
Zasilaczccz
Amperomierz
1 cm
…
... zobacz całą notatkę






Komentarze użytkowników (0)