To tylko jedna z 47 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


Enzymologia
E
l i
Wykład 11
Wykład 11
Enzymy jako reagenty chemiczne
Enzymy jako reagenty chemiczne
Literatura
Biotransformations in organic synthesis – K. Faber (Springer,
2004)
y
g
y
J
Hydrolases in organic synthesis – R.J. Kazlauskas,
U.T.Bornscheuer (Wiley, 2006)
Biocatalysis – fundamentals and applications – A S Bommarius
and applications A.S. Bommarius,
B.R. Riebel (Wiley, 2004)
Enzyme catalysis i organic synthesis – K D
E
t l i in
i
th i K. Drauz, H. Waldmann
H W ld
(Wiley, 2002)
Applied Biocatalysis – A.J.J. Straathof, P. Adlercreutz (HAP, 2000)
y
(
y
)
Carrierbound immobilized enzymes – L. Cao (Wiley, 2005)
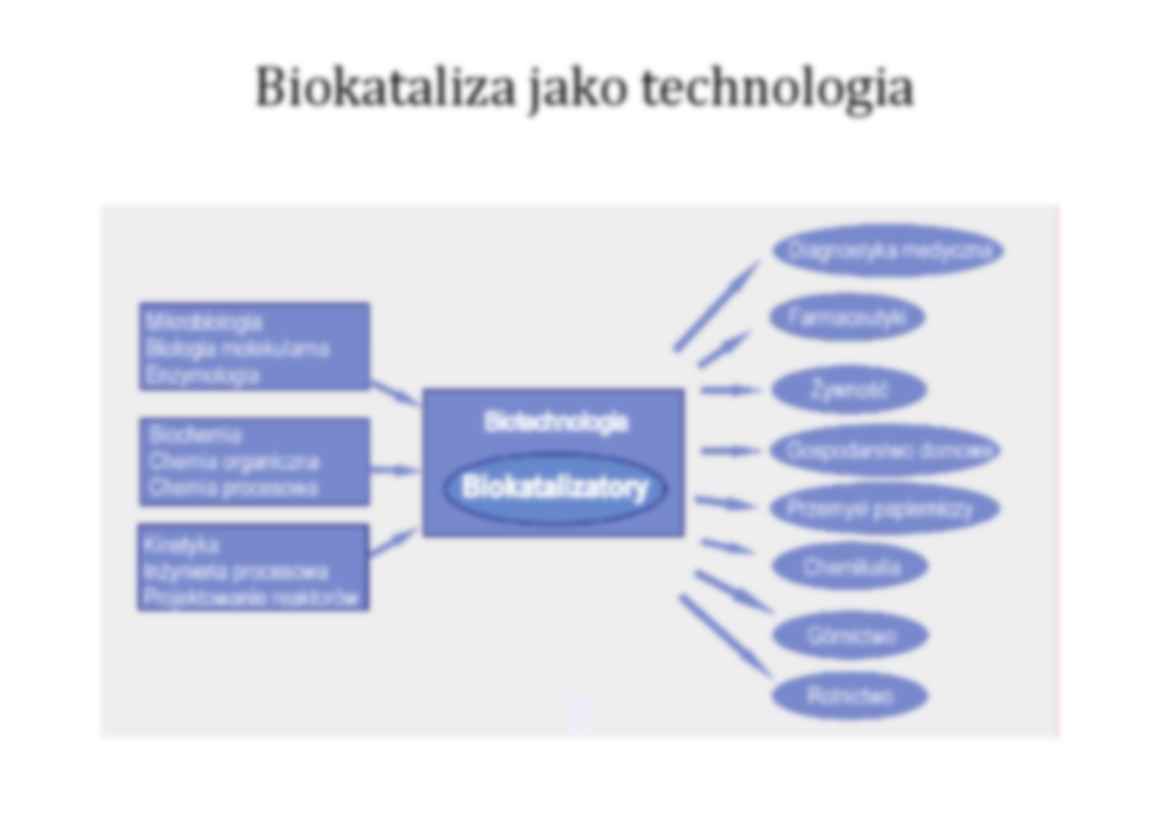
Biokataliza jako technologia
Zalety biokatalizy
Wysoka chemo‐, regio‐, stereo‐ i enancjoselektywność
Efektywność katalizy – reakcje przebiegają 108‐1015‐razy szybciej,
10 razy
a wystarczy stężenie 10‐3‐10‐4 %mol (chemiczne: 0,1‐1%mol)
Reakcje przebiegają w łagodnych warunkach
Nie zachodzą reakcje uboczne
Reakcje mogą przebiegać w wodzie, jak i w rozpuszczalnikach organicznych
j
gą p
g
,j
p
g
y
Biodegradowalność
Enzymy mogą katalizować każdą
reakcję, wyjątkiem są niektóre
cykloaddycje
Kompatybilność – enzym jest
wybiórczy w stosunku do danego
substratu – synteza „one‐pot”
Dlaczego enzymy są lepsze?
Dlaczego enzymy są lepsze?
Otrzymywanie D‐pantolaktonu
PL – pantolakton
PA – kwas pantoinowy
Wady biokatalizy
Zbudowane tylko z L‐aminokwasów
Ograniczona dostępność
Niska stabilność
Niska stabilność
Wrażliwość na zmiany pH i temperatury
Środowisko wodne mało korzystne ze względów technologicznych
Podatność na inhibicję (np. substratową)
Czasochłonne i kosztowne badania nad nowymi enzymami
Ograniczenie zastosowanie do niektórych reakcji
Ograniczenie zastosowanie do niektórych reakcji
Oczyszczanie może być kłopotliwe
Materiał biologiczny może być szkodliwy dla człowieka i środowiska
Zastosowanie enzymów w syntezie
Reakcje redukcji – redukcja grupy karbonylowej ketonów i ketoestrów,
j
j
j g py
y
j
,
redukcja wiązania podwójnego alkenów ‐ dehydrogenazy i reduktazy
Reakcje utleniania – reakcja Bayera‐Villingera, utlenianie sulfidów,
Bayera Villingera,
hydroksylacja alkenów, epoksydacja ‐ monooksygenazy, dioksygenazy,
oksydazy
Reakcje hydrolizy, estryfikacji i transestryfikacji – synteza estrów,
amidów, kwasów karboksylowych, alkoholi – esterazy, lipazy, proteazy,
nitrylazy, hydrolazy epoksydów
Tworzenie wiązania węgiel‐węgiel – reakcja aldolowa, reakcja
Michaela, addycja CN ‐ aldolazy, transketolazy, oksynitrylazy
Reakcje halogenowania i dehalogenowania ‐ haloperoksydazy
j
g
g
p
y y
Zastosowanie biokatalizatorów
Dostępność enzymów jest najczęściej limitującym etapem w projektowaniu
biotransformacji.
Najczęściej stosowane są hydrolazy ale przydatne są też oksydoreduktazy
hydrolazy,
oksydoreduktazy.
Tanie preparaty enzymatyczne są produkowane generalnie na potrzeby
detergentów lub przemysłu spożywczego, ale z powodzeniem mogą być
g
p
y
p y
g
p
gą y
wykorzystywane w syntezie.
Zastosowanie biokatalizatorów
Specyficzność
... zobacz całą notatkę






Komentarze użytkowników (0)