To tylko jedna z 3 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


Grupa: Zespół: Ćwiczenie nr 4
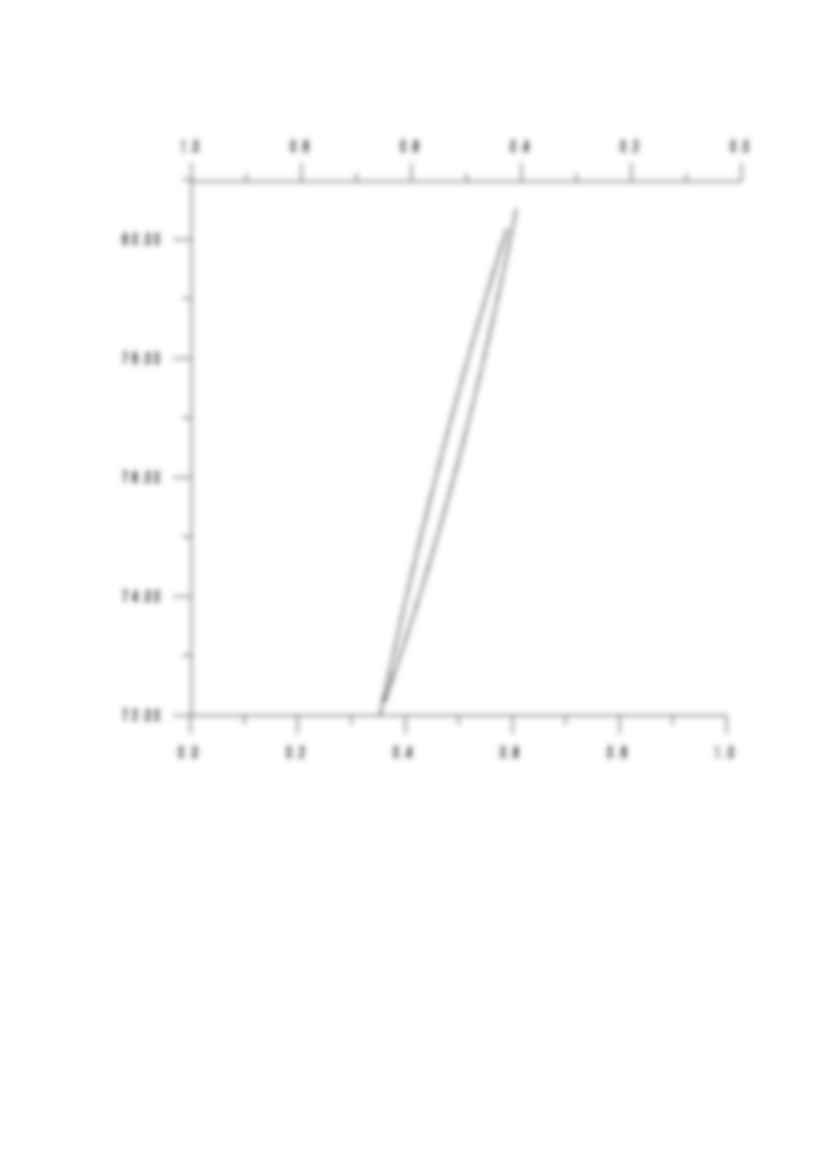
Data: Destylacja. Wyznaczanie krzywych równowagowych ciecz - para
Ocena:
Wstęp
W roztworze zawierającym rozpuszczalnik i substancję rozpuszczoną potencjał chemiczny składnika w każdej fazie jest funkcją temperatury, ciśnienia i ułamka molowego w tej fazie. W stanie równowagi potencjały we wszystkich fazach są sobie równe:
Wychodząc od tego założenia można wyprowadzić wzór na prawo Raoulta:
Prawo to mówi, że prężność pary nad roztworem jest równe prężności pary nad czystym rozpuszczalnikiem pomnożonej przez ułamek molowy rozpuszczalnika. Prawo to jest spełnione przez roztwory doskonałe. Wtedy wykres zależności prężności od zmiany składu jest linią prostą. W przypadku roztworów rzeczywistych krzywa ciśnienia jako funkcji składu odbiega od linii prostej i możliwe są dwa rodzaje odchyleń: dodatnie i ujemne. Odchylenia dodatnie mają miejsce, gdy sumaryczna prężność pary nad roztworem jest większa niż wynikałoby to z prawa Raoulta. Gdy prężność pary nad roztworem jest mniejsza niż wynikająca z prawa Raoulta, wówczas mamy do czynienia z odchyleniami ujemnymi. Czasami odchylenia te są tak duże, że krzywe zależności prężności pary od zmiany składu przyjmują ekstrema. Wtedy mówimy o azeotropii. Gdy roztwory wykazują odchylenia niewielkie, wtedy nazywamy je zeotropami. Odchylenia te są spowodowane oddziaływaniami między cząsteczkami A-A, B-B, a A-B. Jeżeli przyciąganie między cząsteczkami tego samego typu (A-A, B-B) jest większe niż między cząsteczkami różnego rodzaju (A-B), to występują odchylenia dodatnie. W przeciwnym przypadku, gdy (A-A),(B-B)
... zobacz całą notatkę






Komentarze użytkowników (0)