To tylko jedna z 4 stron tej notatki. Zaloguj się aby zobaczyć ten dokument.
Zobacz
całą notatkę


INSTRUKCJA DO ĆWICZENIA
Analiza termiczna
Cele ćwiczenia:
Celem ćwiczenia jest sporządzenie i omówienie diagramu równowag fazowych ciecz ciało stałe
układu dwuskładnikowego Bi-Sn.
Analiza termiczna polega na ogrzewaniu lub chłodzeniu ze stałą szybkością mieszaniny
o stałym składzie i obserwacji przebiegu zmian temperatury na krzywych temperatura-czas,
wskazujących na istnienie przemian fazowych. Załamania te spowodowane są wydzielaniem lub
pochłanianiem ciepła, które towarzyszy każdej przemianie fazowej. Stałą szybkość chłodzenia
uzyskuje się dzięki dużej różnicy temperatur układu i otoczenia. Zaletą analizy termicznej jest
możliwość badania przemian fazowych w wysokich temperaturach. Szczególnie nadaje się ona do
badania diagramów fazowych układów o dużym przewodnictwie cieplnym.
T A
1
2
3
4
5
T
TmB
TmA
L
L+α
L+β
α
β
α+β
τ
A
1
F
2
3
4
5G
B
H
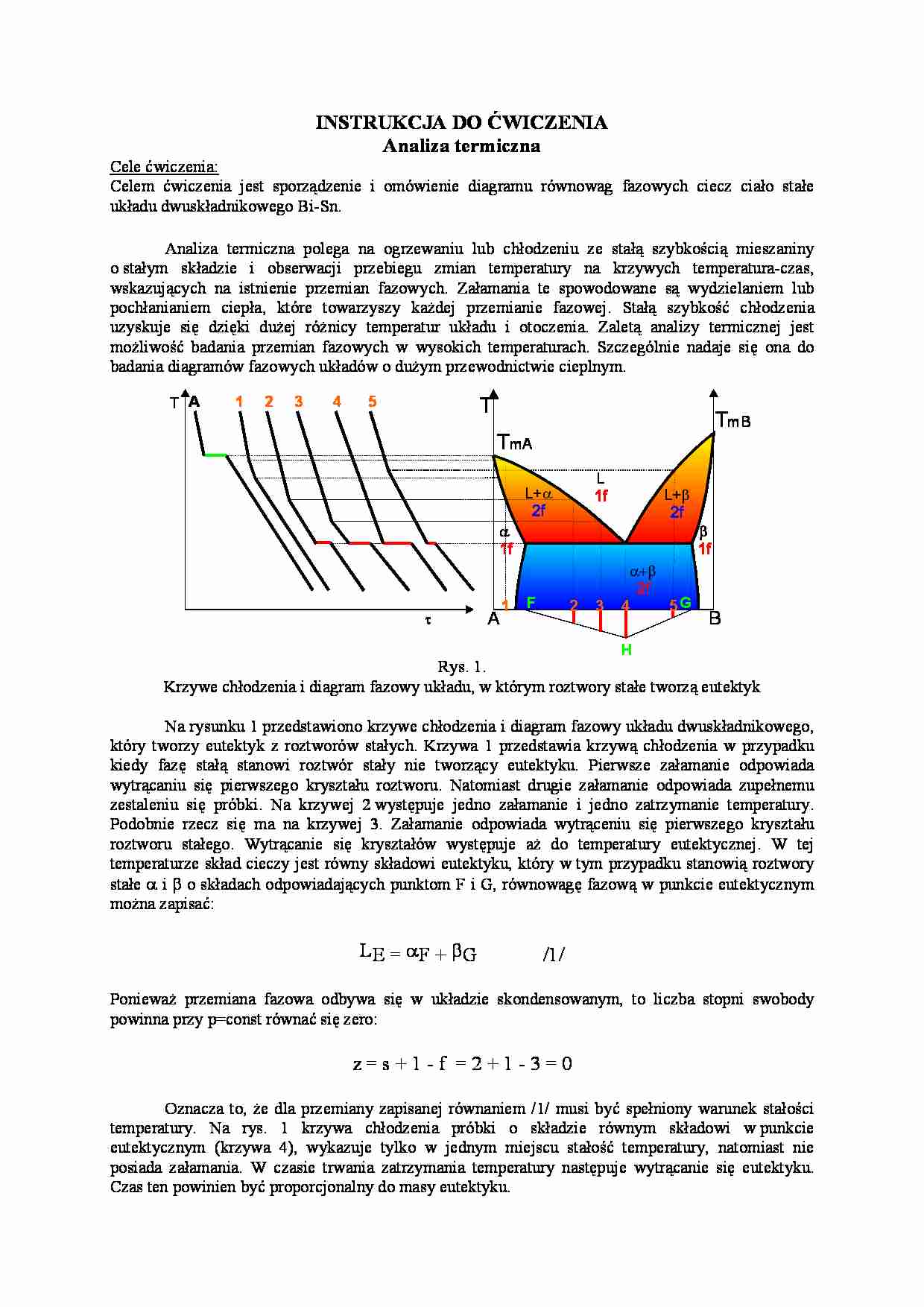
Rys. 1.
Krzywe chłodzenia i diagram fazowy układu, w którym roztwory stałe tworzą eutektyk
Na rysunku 1 przedstawiono krzywe chłodzenia i diagram fazowy układu dwuskładnikowego,
który tworzy eutektyk z roztworów stałych. Krzywa 1 przedstawia krzywą chłodzenia w przypadku
kiedy fazę stałą stanowi roztwór stały nie tworzący eutektyku. Pierwsze załamanie odpowiada
wytrącaniu się pierwszego kryształu roztworu. Natomiast drugie załamanie odpowiada zupełnemu
zestaleniu się próbki. Na krzywej 2 występuje jedno załamanie i jedno zatrzymanie temperatury.
Podobnie rzecz się ma na krzywej 3. Załamanie odpowiada wytrąceniu się pierwszego kryształu
roztworu stałego. Wytrącanie się kryształów występuje aż do temperatury eutektycznej. W tej
temperaturze skład cieczy jest równy składowi eutektyku, który w tym przypadku stanowią roztwory
stałe α i β o składach odpowiadających punktom F i G, równowagę fazową w punkcie eutektycznym
można zapisać:
LE = αF + βG
/1/
Ponieważ przemiana fazowa odbywa się w układzie skondensowanym, to liczba stopni swobody
powinna przy p=const równać się zero:
z=s+1-f =2+1-3=0
Oznacza to, że dla przemiany zapisanej równaniem /1/ musi być spełniony warunek stałości
temperatury. Na rys. 1 krzywa chłodzenia próbki o składzie równym składowi w punkcie
eutektycznym (krzywa 4), wykazuje tylko w jednym miejscu stałość temperatury, natomiast nie
posiada załamania. W czasie trwania zatrzymania temperatury następuje wytrącanie się eutektyku.
Czas ten powinien być proporcjonalny do masy eutektyku.
Na wymienionym fakcie opiera się graficzna metoda wyznaczania składu eutektyku podana w
roku 1903 przez Tammana. Jeżeli będziemy obserwować przebieg krzywych chłodzenia próbek o
takiej samej masie, w tym samym układzie i chłodzonych z tą samą prędkością, to odkładając czas
trwania stałości temperatury w zależności od składu próbki otrzymamy trójkąt, którego wierzchołek H
(rys. 1) odpowiada składowi eutektyku.
Dla wyżej omówionego układu można wyznaczyć, za pomocą graficznej metody Tammana,
skład eutektyku i roztworów ten eutektyk tworzących. Trójkąt Tammana został przedstawiony na rys.
1
... zobacz całą notatkę






Komentarze użytkowników (0)