Rozwiązania zadań egzaminacyjnych z chemii fizycznej sem. 4
© Włodzimierz Tszyrsznic
KINETYKA
P in mmHG = 7,50*10-3 ciśnienia w Pa
zad.
Badając
spektroskopowo
izomeryzację
pierwszego
rzędu
chlorku
cis-dwuetylenodwuaminodwuchlorokobaltu (III) w metanolu, otrzymano następujące dane
dotyczące szybkości znikania piku absorpcyjnego odpowiadającego długości fali 540 nm jako
funkcji czasu:
czas/min
0
absorbancja 0,119
10
0,115
20
0,108
33
0,102
47
0,096
62
0,089
80
0,081
93
0,075
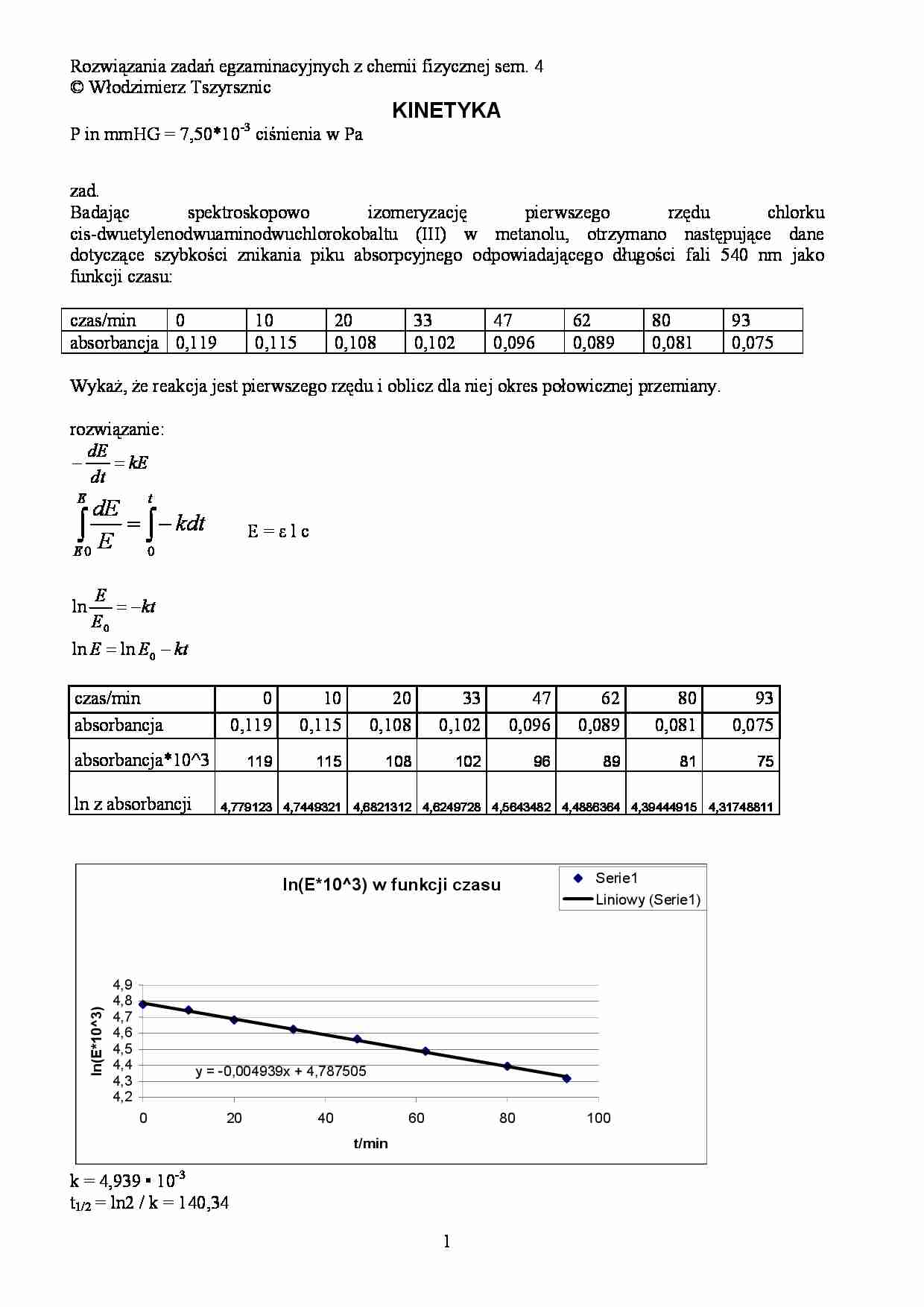
Wykaż, że reakcja jest pierwszego rzędu i oblicz dla niej okres połowicznej przemiany.
rozwiązanie:
dE
−
= kE
dt
E
t
dE
∫0 E = ∫ − kdt
0
E
ln
E=εlc
E
= − kt
E0
ln E = ln E0 − kt
czas/min
absorbancja
0
0,119
10
0,115
20
0,108
33
0,102
47
0,096
62
0,089
80
0,081
93
0,075
119
115
108
102
96
89
81
75
absorbancja*10^3
ln z absorbancji
4,779123 4,7449321 4,6821312 4,6249728 4,5643482 4,4886364 4,39444915 4,31748811
ln(E*10^3)
ln(E*10^3) w funkcji czasu
4,9
4,8
4,7
4,6
4,5
4,4
4,3
4,2
Serie1
Liniowy (Serie1)
y = -0,004939x + 4,787505
0
20
40
60
80
t/min
k = 4,939 • 10-3
t1/2 = ln2 / k = 140,34
1
100
Rozwiązania zadań egzaminacyjnych z chemii fizycznej sem. 4
© Włodzimierz Tszyrsznic
R2 = 0,997835
zad.
W temperaturze 230ºC badano reakcję otrzymywania butadienu w wyniku statycznego efektu
sprzężenia:
CH2=CH-CH2-CH3
Cr 2 O
CH2=CH-CH=CH2 + H2
3
mierząc ciśnienie całkowite (p) w różnych odstępach czasu w układzie o stałej objętości:
Uzyskano następujące wyniki:
t/min
p/mmHg
0
116
5
123
7
125,5
9
128,7
∞
12,5
133
232
Sprawdź, czy reakcja jest pierwszego rzędu i obliczyć stałą szybkości.
Rozwiązanie:
t/min
0
pSUMARYCZNE/Tr
pA/Tr
ln(pA)
1/pA
1/pA^2
5
116
123
116
109
4,75359 4,691348
8,621E-03 9,174E-03
7,432E-05 8,417E-05
7
9
125,5
128,7
106,5
103,3
4,668145 4,637637
9,390E-03 9,681E-03
8,817E-05 9,371E-05
∞
12,5
133
232
99
0
4,59512 -----------1,010E-02 -----------1,020E-04 ------------
PSUMARYCZNE = 2 PPoczA - PA
PA = - PSUMARYCZNE + 2 PpoczA
I rzędu
4,78
4,76
4,74
4,72
4,7
4,68
4,66
y = -0,0127x + 4,7545
R2 = 0,999
4,64
4,62
4,6
4,58
0
2
4
6
8
10
12
14
II rzędu
1,020E-02
III rzędu
y = 0,00000222x + 0,00007360
1,200E-04
R2 = 0,99482833
1,000E-04
y = 0,0001x + 0,0086
2
R = 0,9976
1,000E-02
9,800E-03
9,600E-03
8,000E-05
9,400E-03
6,000E-05
9,200E-03
9,000E-03
4,000E-05
8,800E-03
2,000E-05
8,600E-03
0,000E+00
8,400E-03
0
2
4
6
8
10
12
0
14
2
5
10
15
Rozwiązania zadań egzaminacyjnych z chemii fizycznej sem. 4
© Włodzimierz Tszyrsznic
Reakcja jest pierwszego rzędu.
zad.
Stwierdzono, że katalizowana reakcja równoległego nitrowania toluenu do mononitropochodnych o, p-, m- przebiega jako reakcja pierwszego rzędu. Po 20 minutach zużyte zostało 40% substratu. W
produktach stwierdzono następujące ilości: -o (70%), p-(20%), m-(10%). Obliczyć stałe szybkości
reakcji otrzymywania trzech pochodnych.
Rozwiązanie:
Orto
ko
km
Substrat
Meta
kp
Para
time = 20 min
zużyto: 40%, więc pozostało:
... zobacz całą notatkę





Komentarze użytkowników (0)